Urolitiasis pediatrica
Prasad Godbole
Sheffield Children’s NHS Foundation Trust, Sheffield, UK
Traducido y editado desde el original al español | Enlace a la versión en inglés
Dra Maria Santos, Dra Carolina Acuña
Hospital Padre Hurtado, Santiago Chile
Introducción
La urolitiasis pediátrica es poco común en Europa occidental, con una incidencia en el Reino Unido menor a 2 por millón de habitantes, pero se encuentra con mayor frecuencia en el "Stone Belt" regiones del mundo caracterizadas por una prevalencia de urolitiasis de 10 a 15%. En países con urolitiasis endémica, los cálculos vesicales eran mucho más prevalentes, pero con la industrialización, esta incidencia está disminuyendo.
Epidemiología
La incidencia de cálculos del tracto urinario ha aumentando, afectando a niños por sobre las niñas. La gran mayoría de los cálculos se encuentran en el tracto urinario superior.
Fisiopatología
La fisiopatología de la litiasis es multifactorial y está determinada por una combinación de factores como son el flujo y volumen de orina, saturación de cristales en orina y pH urinario. Cualquier factor que afecte a estos componentes puede dar lugar a cálculos en el tracto urinario (consulte la Figura 1 a continuación)
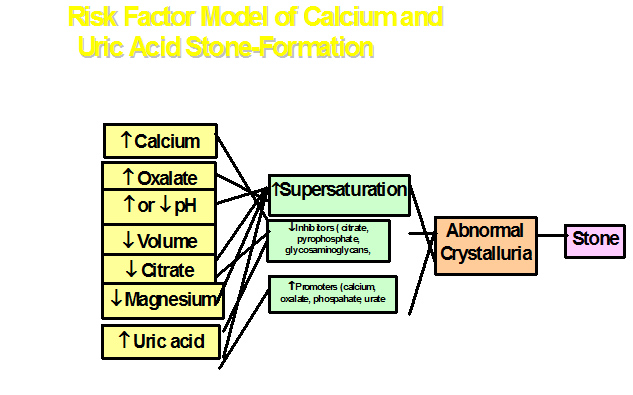
Figura 1. Modelo de factores de riesgo para la producción de calcio y ácido úrico en orina.
Figura 1. Modelo de factores de riesgo para la producción de calcio y ácido úrico en orina.
El primer prerequisito para la formación de cálculos es la sobresaturación de orina. La cristalización se produce debido a una sobresaturación asociada a un desequilibrio entre los promotores (aumento) y los inhibidores (disminución) Los promotores son principalmente calcio, oxalato, fosfato y urato. Los inhibidores son citrato, pirofosfato, glicosaminoglicanos y glicoproteínas. Tras la sobresaturación, se forman cristales en el lumen de los túbulos, los cuales pueden agregarse. Si hay trastornos metabólicos subyacentes o causas dietéticas, también pueden causar sobresaturación. La diuresis deficiente puede agravar la sobresaturación. La infección urinaria, particularmente debida a organismos productores de ureasa, causa alcalinización de la orina y cristalización / sobresaturación de varios compuestos como la estruvita o carbapatita y urato de amonio.
Los cálculos se pueden encontrar tempranamente en el período postnatal de recién nacidos prematuros a los que se les ha administrado furosemida para su enfermedad pulmonar crónica. Esta condición, mas que una litiasis propiamente tal, se conoce como nefrocalcinosis donde los cristales se depositan en el intersticio medular del parénquima renal, más que en el sistema colector.
Diagnóstico
El diagnóstico de cálculos en los niños requiere de un alto índice de sospecha, ya que las características de presentación son múltiples y variables. En cualquier grupo etario, los síntomas pueden ser los de una infección del tracto urinario como disuria, frecuencia, hematuria y paso de arenilla o cálculos pequeños o matriz. Esto puede ir acompañado de dolor. En lactantes, la litiasis puede manifestarse con letargo, irritabilidad, inapetencia y fiebre.
La confirmación del diagnóstico se basa en imágenes adecuadas. En los niños, la imagen de elección es la ecografía renal junto con una radiografía abdomen simple. La ultrasonografía renal es sensible, específica y puede detectar cálculos en todo el tracto urinario. En el riñón, puede demostrar la ubicación de los cálculos en el sistema colector. Sin embargo, es operador dependiente y puede no visualizar cálculos en el uréter medio o el uréter distal, especialmente si está oculto por el gas intestinal y si la vejiga está vacía. La radiografía abdominal simple es un complemento útil para la detección de cálculos. Sin embargo, la carga fecal / gas intestinal pueden contaminar la imagen y, por lo tanto, la radiografía simple no es tan sensible como la ecografía.
Frente a pacientes en los que hay un alto índice de sospecha pero no logran visualizarse cálculos con ultrasonido más radiografía convencional, se puede recurrir a otras modalidades de imágenes. En estos casos, una tomografía computada helicoidal sin medio de contraste puede demostrar la presencia de un cálculo. Las imágenes funcionales antes de cualquier intervención son importantes y el autor sugiere solicitar, de manera rutinaria, una cintigrama DMSA antes de cualquier intervención. Al momento del cintigrama DMSA, vale la pena obtener una Pielografia Endovenosa (IVU) para demostrar la anatomía calicial ya que esto puede orientar el enfoque, especialmente si se está considerando una nefrolitotomía percutánea NLPC
Naturaleza de los cálculo
la naturaleza y la composición de los cálculos pueden influir en la elección del tipo de intervención y el éxito del procedimiento. Las piedras de cistina son, sin duda, de consistencia muy dura y, por ende, difíciles de desintegrar y son, además, muy poco radio opacas. Los cálculos de estruvita normalmente tienen suficiente fosfato de calcio, lo que las hace radio opacas. Los litos de ácido úrico son radiolúcidos y las piedras de oxalato de calcio son las más radio opacas.
Evaluación
Ante la sospecha de urolitiasis, se debe realizar una historia clínica completa que incluya una historia dietética. La historial familiar de trastornos metabólicos y/o litiasis es importante. Debe abordarse también, cualquier historia urológica que pueda predisponer a la formación de cálculos, como una cistoplastia de aumento. La evaluación de laboratorio debe incluir orina completa más urolcultivo y análisis bioquímicos de la sangre. Las muestras de sangre deben incluir electrolitos plasmáticos, creatininemia, calcio, fosfato y ácido úrico. El análisis de orina generalmente se realiza en una recolección de orina de 24 horas, aunque la mayoría de los laboratorios ahora pueden realizar la evaluación en una muestra única de orina. La orina debe analizarse en busca de calcio, oxalato, ácido úrico, citrato y sodio y potasio en orina. La relación Calcio/Creatinina y Oxalato/Creatinina también debe medirse. El elemento más importante de la evaluación es el análisis de la composición química del cálculo, de tal manera de determinar la etiología.
Manejo Médico
En los niños con urolitiasis, el objetivo principal es el manejo quirúrgico, con eliminación completa de la carga de cálculos. La única indicación para manejo médico sería después de la remoción de un cálculo grande que deja residuo de pequeños fragmentos en los que se puede esperar que pasen espontáneamente. Esto se denomina "fragmentos residuales clínicamente insignificantes". De manera similar, en la nefrocalcinosis o calcificación en el intersticio, se puede implementar una política de vigilancia y espera, ya que en la mayoría de estos casos, los depósitos cálcicos pueden no progresar e, incluso, en el caso de la nefrocalcinosis, pueden resolverse espontáneamente. Por otra parte, podríamos encontrar una pequeña piedra ureteral de menos de 4 mm de diámetro en ausencia de síntomas. En estos casos, la dilatación proximal puede anticipar el posible paso espontáneo. Aquí el manejo médico con alfa bloqueadores, como Tamsulosina, usado normalmente en adultos, puede relajar la unión uretero – vesical permitiendo el paso del cálculo.
Manejo Quirúrgico
Técnicas mínimamente invasivas: Nefrolitotomía percutánea NLPC, Litotripsia extracorpórea LEC, Ureterorenoscopia URS, laparoscopia.
Cirugía abierta: la cirugía abierta rara vez está indicada para la urolitiasis pediátrica, ya que la mayoría de los cálculos se pueden manejar mediante técnicas mínimamente invasivas, ya sea aisladas o combinadas. Un caso en que la cirugía abierta puede estar indicada es una obstrucción pieloureteral con formación secundaria de cálculos, pero incluso en tales situaciones, la laparoscopia se puede usar con una excelente visualización.
NLPC: la mayor parte de la experiencia en nefrolitotomía percutánea viene de su uso en adultos. Sin embargo, la mejora del instrumental y el menor tamaño de ellos, ha permitido que esta técnica se use en la mayoría de los niños. La NLPC se puede utilizar como monoterapia o en combinación con LEC.
Indicaciones
- Gran carga litiásica, por ejemplo, cálculos coraliformes
- Cálculo único > 2 cm de tamaño
- Cálculos múltiples
- Cálculo de composición dura, no susceptible de desintegración por LEC
Estudios Imageneológicos preoperatorios
Ultrasonografia y Radiografía convencional: esto permite la localización precisa de cálculos renales y puede ayudar a planificar la intervención. (Figuras 2 y 3)
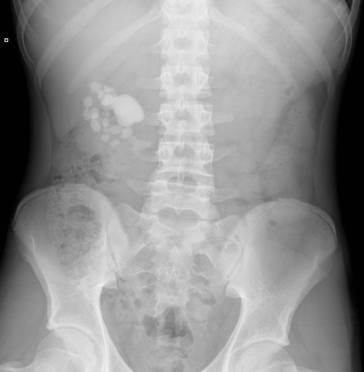
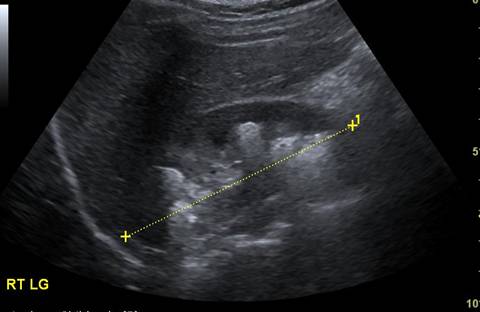
Figuras 2 y 3. Radiografía simple que muestra múltiples cálculos en el riñón derecho en un niño con cistinuria. Ultrasonido que muestra múltiples cálculos en el riñón susceptibles a NLPC
Pielografia Endovenosa (IVU): esto demuestra la anatomía calicilar y la ubicación de los cálculos dentro del sistema colector. Las variaciones anatómicas, como los sistemas dúplex o los sistemas bífidos, también se pueden detectar antes de la operación.
DMSA: puede realizarse a través del mismo sitio de inyección de la IVU y nos da la función del riñón. Cuando el riñón tiene una función deficiente (<10%), la nefrectomía puede ser la alternativa y la mejor intervención.
- Stent ureteral preoperatorio mediante cistoscopia. La punta del stent ureteral se coloca al nivel de la unión pieloureteral. Se inserta una sonda Foley y el stent se sujeta a la sonda para evitar su desplazamiento. Luego se realiza un estudio retrógrado para visualizar la anatomía (Figura 4)
- El paciente se posiciona en prono con el lado afectado a 30-45 grados de elevación. Esto lleva al extremo del cáliz posterior hacia la dirección de la punción.
- Punción: esta puede realizarse mediante control fluoroscópico o de ultrasonografía según la preferencia de los radiólogos intervencionales. En la mayoría de los casos, utilizamos la aguja de Kellett para perforar el cáliz posterior del polo inferior. La inyección de solución salina con azul de metileno diluido a través del catéter retrógrado permite la confirmación de la punción del sistema colector.
- A continuación se posiciona una guía con punta AJ a través de la aguja de punción siendo ideal que baje por el uréter. Si esto resulta difícil, se puede usar una guía hidrofilia (HiWire) y luego reemplazarla con la guía en forma de J.
- El tracto se dilata al tamaño requerido. La dilatación puede ser con un dilatador de balón como en pacientes adultos. Preferimos el uso de dilatadores metálicos seriados (Alken) ya que creemos que dilatan el tracto gradualmente en lugar de la dilatación radial repentina con el dilatador de balón. La posición de los dilatadores se comprueba mediante fluoroscopía. Luego se inserta una vaina Amplatz de 24 o 26F sobre el dilatador final, su posición se confirma con fluoroscopía y se retiran los dilatadores. (Figura 5)
- El cálculo se visualiza a través del nefroscopio y se desintegra con un litotriptor de ultrasonido, litoclast o láser y los fragmentos son recuperados mediante pinzas de agarre o canastillos.
- Puede requerirse una segunda punción, ya sea durante el mismo procedimiento o en una sesión separada si no se logra extracción completa del cálculo y sus fragmentos.
- Se coloca una nefrostomía 8F y se retira la vaina de Amplatz.
- La nefrostomía se clampea 24 horas después del procedimiento y se retira a las 36 horas.
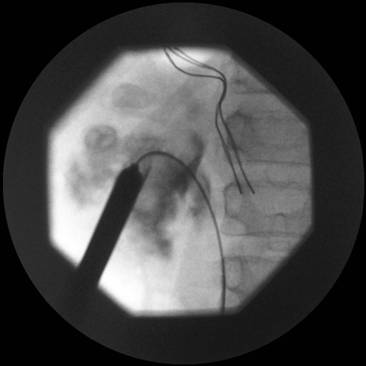
Figura 5. Imagen que muestra la guía hacia abajo en el uréter derecho, la vaina de amplatz en posición y los dilatadores de metal que se están retirando.
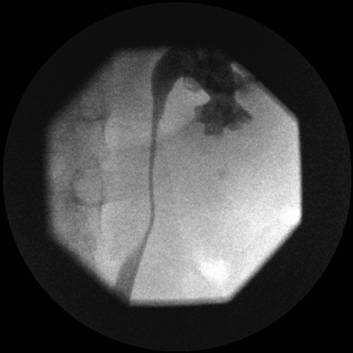
Figura 4. Pielografía retrógradas que demuestra cálculos predominantemente en el polo inferior que permiten la punción del cáliz apropiado.
LEC (litotricia extracorpórea por ondas de choque)
La generación de ondas de choque a través de variadas técnicas y el foco de estas ondas sobre un solo punto en el manejo de los cálculos se ha llevado a cabo durante las últimas dos décadas. La primera LEC se realizó en Alemania en 1980. El principio detrás de la LEC incluye 3 elementos:
- generación de la onda de choque
- foco de la onda de choque
- desintegración del cálculo
La onda de choque puede ser generada por una de siguientes tres técnicas:
- Litotriptor electrohidráulico
- Lithrotripter piezoeléctrico
- Litotriptor electromagnético
Litotriptor electrohidráulico
Esto utiliza el principio de "spark gap" para generar la onda de choque. Dos electrodos se colocan juntos y una corriente de alta energía pasa entre ellos. Esto crea una chispa que causa el desarrollo de una onda de choque en el agua circundante. Esto puede ser enfocado en un objetivo para desintegrar la piedra. El procedimiento requiere que el paciente se sumerja en un baño de agua lo cual hace que el equipo sea voluminoso y engorroso. Además los niveles de energía pueden fluctuar entre las ondas de choque.
Litotriptor piezoeléctrico
Este utiliza cristales cerámicos piezoeléctricos dispuestos en una esfera que se cargan y descargan para crear la onda de choque. Esto se puede enfocar en el objetivo con un nivel de precisión muy alto. Sin embargo, la energía suministrada es relativamente pequeña y requiere tiempos de tratamiento más largos y, a veces, procedimientos repetidos para la fragmentación completa de los cálculos.
Litotriptor electromagnético
Utiliza dos bobinas con campos magnéticos pasados a través de ellos en direcciones opuestas. Estos campos magnéticos opuestos hacen que la membrana laminar adyacente a la bobina vibre, produciendo así la onda de choque. La onda se puede enfocar a través de un lente cóncavo o a través de un lente cilíndrico. La ventaja de este sistema es que los complementos de enfoque, como el ultrasonido y la unidad de fluoroscopía, son parte integral del dispositivo generador de ondas de choque. Este es el litotriptor más utilizado.
Cavitación
Las ondas de choque provocan la desintegración del cálculo mediante cavitación. Esto comienza en el punto de entrada y crea microburbujas por evaporación del aire dentro de la piedra. Estas microburbujas se colapsan y se unen con nuevas microburbujas que forman una onda secundaria. Este proceso progresa a través de toda la piedra hasta que se produce la fragmentación. Este proceso también se produce en la interfaz de la piedra y el tejido adyacente, lo que puede provocar lesiones colaterales.
Ureterorenoscopía (URS)
El advenimiento de los ureteroscopios más pequeños ha hecho posible el manejo de los cálculos ureterales mediante técnicas mínimamente invasivas. Se han descrito varias técnicas de fragmentación de las piedras, incluido el láser Ho: YaG o el litoclast. Siguiendo la introducción preliminar de una guía a través del ostium ureteral, se avanza suavemente el ureteroscopio hacia el uréter más allá de la porción intramural de este. En los casos de un cálculo impactado, la inserción de un stent ureteral doble J durante unas pocas semanas previas puede hacer este procedimiento más fácil. El cálculo se visualiza y se puede estabilizar con un canastillo (como el canastillo de Nitinol). Entonces se puede usar el láser. Es importante asegurarse que el láser esté en contacto directo con la superficie de la piedra antes de la fragmentación. No se puede usar un canastillo si se usa un pequeño ureteroscopio (4.5F) o si se usa una sonda de litoclast. Los fragmentos más grandes se pueden recuperar después de la fragmentación usando el canastillo, pero los fragmentos más pequeños se pueden dejar pasar espontáneamente. La colocación de stents postoperatorios durante una semana puede ser necesaria en el caso de cálculos grandes para permitir que las piedras pasen. No utilizamos de rutina estos stents doble J después de la ureteroscopia y la litrotripsia con láser.
Las principales complicaciones de este procedimiento son las lesiones en la pared del uréter y el desplazamiento del cálculo hasta el riñón.
Laparoscopia
La laparoscopia se puede usar en casos de cálculos solitarios a nivel de pelvis renal, cálculos ureterales impactados o cálculos en un riñón ubicado de manera anormal. La técnica puede tomar mucho tiempo y depende de la experiencia del operador.
Complicaciones
NLPC
- Punción fallida o incapacidad para crear el tracto
- Sepsis
- Hemorragia que requiere transfusión
- Lesión del sistema colector
- Cálculos residuales que requieren más NLPC o LEC
- Fuga urinaria / urinoma
- Conversión a técnica abierta debido a sangrado significativo
LEC
- Hematomas
- Equimosis
- Hematoma perirrenal
- Arritmias
- Lesión pulmonar en caso de localización incorrecta.
- SteinStrasse - debido a la gran carga de cálculos
- Coágulos
- Dolor e incapacidad para tolerar LEC sin anestesia general. En nuestra unidad, la LEC se ofrece a los niños mayores de 12 años sin anestesia. Todos los demás niños requieren anestesia general para el procedimiento.
URS
- Lesión / disrupción del uréter
- Urosepsis
- Fuga urinaria
- Cálculo residual
- Sangrado
- Dolor
Resultados a corto y largo plazo
Las principales medidas de resultado de cualquier intervención quirúrgica para la urolitiasis pediátrica incluyen
Eliminación completa de cálculos – tasa libre de cálculos
Morbilidad Lesión renal a largo plazo Recurrencia
LEC
La seguridad a largo plazo y los efectos biológicos de la LEC sobre la función y crecimiento renal son discutibles. Brinkman et al. no observaron evidencia de cicatrices renales, cambios en la presión sanguinea o pérdida de la función renal en su serie de 63 niños sometidos a LEC. La GFR puede disminuir después de la LEC pero vuelve a la normalidad dentro de los 3 meses. La exposición a la radiación durante la LEC es comparable a otros procedimientos radiográficos de diagnóstico.
Dependiendo de la naturaleza del cálculo, de su posición y de la anatomía calicial, las tasas libre de cálculos varían entre 75-80% en varias series. Se pueden requerir sesiones múltiples para obtener un mayor porcentaje de eliminación. La colocación de stent no suele ser necesaria en niños. Cuando hay una alta carga de cálculos, las tasas libre de cálculos varían entre 33-80%. La morbilidad a corto plazo se describe anteriormente. Las tasas libre de cálculos varían entre 75 y 100% para los litos ureterales dependiendo de la incapacidad para localizar la piedra.
NLPC
Los estudios demuestran una cicatrización mínima y una pérdida insignificante de la función renal después de NLPC. La hemorragia intraoperatoria está relacionada con la cantidad de vías de acceso y el calibre de la misma. Las vías múltiples pueden aumentar la pérdida de sangre, pero no están relacionadas con un mayor riesgo de complicaciones.
Las tasas de eliminación con NLPC como monoterapia o como parte de la terapia de sándwich alcanzan tasas de eliminación de entre el 85 y el 96%.
URS
La dilatación ureteral no aumenta el riesgo de estenosis y el reflujo vesicoureteral significativo después de la ureteroscopia. La incidencia de RVU de bajo grado puede ser tan alta como 15% después de los procedimientos ureteroscópicos.
Comentario editorial
El manejo de la urolitiasis pediátrica ha avanzado mucho en las últimas dos décadas. Las mejoras en la tecnología han jugado un papel importante en este desarrollo. Para que el manejo de esta patología tenga éxito, se requiere un especialista dedicado y preparado para dirigir el equipo multidisciplinario. Además, estos procedimientos toman tiempo especialmente en el periodo de la curva de aprendizaje y todo el equipo debe estar preparado para esto.
En términos de tecnología, las antiguas vainas Amplatz de 24 o 26 Fr resultan ser difíciles y posiblemente traumáticas para los riñones infantiles. La llegada del kit de miniperc, con fundas tan pequeñas como 11 Fr y un mini nefroscopio, han permitido que esto se use en niños pequeños. Sin embargo, esta técnica requiere el uso de un láser que, en casos de una gran carga litiasica puede llevar mucho tiempo para despejarse.
No hace falta decir que este servicio no se puede conformar y tener éxito sin tener todo el equipo requerido, incluidos los insumos extras. En nuestro servicio, tenemos los kits para adultos y mini perc, incluidos nefroscopios, ureteroscopio flexible y semirrígido, cistoscopio flexible, láser, litoclast suizo, una selección de guías (incluidoas las hidrófílicas), un catéter de cobra (vascular) y una gama de canastillos, pinzas, etc. nada puede ser más frustrante que poder visualizar un cálculo pero no ser capaz de extraerlo debido a una anatomía incómoda y a la falta del instrumental adecuado.
Referencias
1: Badawy AA, Saleem MD, Abolyosr A, Aldahshoury M, Elbadry MS, Abdalla MA, Abuzeid AM. Extracorporeal shock wave lithotripsy as first line treatment for urinary tract stones in children: outcome of 500 cases. Int Urol Nephrol 2012. 2: Baştuğ F, Düşünsel R. Pediatric urolithiasis: causative factors, diagnosis and medical management. Nat Rev Urol 2012 Feb 7. 3: Baştuğ F, Gündüz Z, Tülpar S, Poyrazoğlu H, Düşünsel R. Urolithiasis in infants: evaluation of risk factors. World J Urol 2012 Jan 19. 4: Desai M. Treatment of pediatric urolithiasis: how small is "small enough"? World J Urol 2011; 29:705-6 5: Goktas C, Akca O, Horuz R, Gokhan O, Albayrak S, Sarica K. SWL in lower calyceal calculi: evaluation of the treatment results in children and adults. Urology 2011; 78: 1402-6. 6: Habbig S, Beck BB, Hoppe B. Nephrocalcinosis and urolithiasis in children. Kidney Int 2011; 80: 1278-91. 7: Dogan HS, Onal B, Satar N, Aygun C, Piskin M, Tanriverdi O, Gurocak S, Gunay LM, Burgu B, Ozden E, Nazli O, Erdem E, Yucel S, Kefi A, Demirci D, Uluocak N, Aridogan IA, Turunc T, Yalcin V, Kilinc M, Horasanli K, Tan MO, Soygur T, Sarikaya S, Kilicarslan H, Turna B, Doruk HE, Tekgul S. Factors affecting complication rates of ureteroscopic lithotripsy in children: results of multi-institutional retrospective analysis by Pediatric Stone Disease Study Group of Turkish Pediatric Urology Society. J Urol 2011; 186: 1035-40. 8: Sas DJ. An update on the changing epidemiology and metabolic risk factors in pediatric kidney stone disease. Clin J Am Soc Nephrol 2011; 6: 2062-8. 9: Schissel BL, Johnson BK. Renal stones: evolving epidemiology and management. Pediatr Emerg Care 2011; 27: 676-81. 10: Chang HY, Hsu CH, Tsai JD, Li ST, Hung HY, Kao HA, Chang JH, Chung HY, Wang HK. Renal calcification in very low birth weight infants. Pediatr Neonatol 2011; 52: 145-9. 11: Polito C, Apicella A, Marte A, Signoriello G, La Manna A. Clinical presentation and metabolic features of overt and occult urolithiasis. Pediatr Nephrol 2012; 27: 101-7. 12: Desai MR, Sharma R, Mishra S, Sabnis RB, Stief C, Bader M. Single-step percutaneous nephrolithotomy (microperc): the initial clinical report. J Urol 2011; 186: 140-5. 13: Kumar R, Anand A, Saxena V, Seth A, Dogra PN, Gupta NP. Safety and efficacy of PCNL for management of staghorn calculi in pediatric patients. J Pediatr Urol 2011; 7: 248-51. 14: Panfeng S, Hong C, Zhongjin Y, Wei Z, Wenhui L, Baoguang S, Junsheng B, Liingjun Z, Zizhen H. Management of pediatric urolithiasis induced by melamine-contaminated powdered formula (report of 619 cases). Urology 2011; 78: 411-6. 15: Mishra S, Sharma R, Garg C, Kurien A, Sabnis R, Desai M. Prospective comparative study of miniperc and standard PNL for treatment of 1 to 2 cm size renal stone. BJU Int 2011; 108: 896-9; discussion 899-900. doi:10.1111/j.1464-410X.2010.09936.x. 16: Raju GA, Norris RD, Ost MC. Endoscopic stone management in children. Curr Opin Urol 2010; 20: 309-12. 17: Dillman JR, Kappil M, Weadock WJ, Rubin JM, Platt JF, DiPietro MA, Bude RO. Sonographic twinkling artifact for renal calculus detection: correlation with CT. Radiology 2011; 259: 911-6. 18: Rizvi SA, Sultan S, Ijaz H, Mirza ZN, Ahmed B, Saulat S, Umar SA, Naqvi SA. Open surgical management of pediatric urolithiasis: A developing country perspective. Indian J Urol 2010; 26: 573-6. 19: Reddy PP, Defoor WR. Ureteroscopy: The standard of care in the management of upper tract urolithiasis in children. Indian J Urol 2010; 26: 555-63. 20: Ganpule AP, Mishra S, Desai MR. Percutaneous nephrolithotomy for pediatric urolithiasis. __ 2010; 26: 549-54. 21: Zhu J, Phillips TM, Mathews RI. Operative management of pediatric urolithiasis. Indian J Urol 2010; 26: 536-43. 22: Sharma AP, Filler G. Epidemiology of pediatric urolithiasis. Indian J Urol 2010; 26: 516-22. 23: Ansari MS. Pediatric urolithiasis: A challenging problem. Indian J Urol 2010; 26: 515. 24: Cortes JA, Motamedinia P, Gupta M. Update on technological and selection factors influencing shockwave lithotripsy of renal stones in adults and children. Curr Opin Urol 2011; 21: 134-40. 25: Hwang K, Mason MD, Peters CA. Clinical practice: surgical approaches to urolithiasis in children. Eur J Pediatr 2011; 170: 681-8. 26: Matlaga BR, Schaeffer AJ, Novak TE, Trock BJ. Epidemiologic insights into pediatric kidney stone disease. Urol Res 2010; 38: 453-7. 27: Porowski T, Kirejczyk JK, Zoch-Zwierz W, Konstantynowicz J, Korzeniecka-Kozerska A, Motkowski R, Laube N. Assessment of lithogenic risk in children based on a morning spot urine sample. J Urol 2010; 184: 2103-8.. 28: DiSandro M. Pediatric urolithiasis: children as little adults. J Urol 2010; 184: 1833-4. 29: Kieran K, Giel DW, Morris BJ, Wan JY, Tidwell CD, Giem A, Jerkins GR, Williams MA. Pediatric urolithiasis–does body mass index influence stone presentation and treatment? J Urol 2010; 184: 1810-5. 30: Routh JC, Graham DA, Nelson CP. Trends in imaging and surgical management of pediatric urolithiasis at American pediatric hospitals. J Urol 2010; 184: 1816-22. 31: Ozkan KU, Bakan V, Mil A, Ozturk S. Ureteroscopic stone management in prepubertal children. Urol Int 2010; 85: 320-3. 32: Routh JC, Graham DA, Nelson CP. Epidemiological trends in pediatric urolithiasis at United States freestanding pediatric hospitals. J Urol 2010; 184: 1100-4. 33: Nelson CP. Extracorporeal shock wave lithotripsy in the pediatric population. Urol Res 2010;38(4):327-31. 34: Thomas JC. How effective is ureteroscopy in the treatment of pediatric stone disease? Urol Res 2010;38(4):333-5. 35: Alaya A, Najjar MF, Nouri A. Pediatric urolithiasis in the central coast of Tunisia: Epidemiologic changes over the past twenty-five years. Saudi J Kidney Dis Transpl 2010; 21: 762-71. 36: Tanriverdi O, Silay MS, Kendirci M, Kadihasanoglu M, Aydin M, Horasanli K, Miroglu C. Comparison of ureteroscopic procedures with rigid and semirigid ureteroscopes in pediatric population: does the caliber of instrument matter? Pediatr Surg Int 2010; 26: 733-8. 37: Cerwinka WH, Kirsch AJ. Magnetic resonance urography in pediatric urology. Curr Opin Urol 2010; 20: 323-9. 38: Sas DJ, Hulsey TC, Shatat IF, Orak JK. Increasing incidence of kidney stones in children evaluated in the emergency department. J Pediatr 2010; 157: 132-7. 39: DeFoor WR, Jackson E, Minevich E, Caillat A, Reddy P, Sheldon C, Asplin J. The risk of recurrent urolithiasis in children is dependent on urinary calcium and citrate. Urology 2010; 76: 242-5. 40: Unsal A, Resorlu B, Kara C, Bozkurt OF, Ozyuvali E. Safety and efficacy of percutaneous nephrolithotomy in infants, preschool age, and older children with different sizes of instruments. Urology 2010; 76: 247-52. 41: Aydogdu O, Burgu B, Gucuk A, Suer E, Soygur T. Effectiveness of doxazosin in treatment of distal ureteral stones in children. J Urol 2009; 182: 2880-4. 42: Passerotti C, Chow JS, Silva A, Schoettler CL, Rosoklija I, Perez-Rossello J, Cendron M, Cilento BG, Lee RS, Nelson CP, Estrada CR, Bauer SB, Borer JG, Diamond DA, Retik AB, Nguyen HT. Ultrasound versus computerized tomography for evaluating urolithiasis. J Urol 2009; 182: 1829-34. 43: Riccabona M, Avni FE, Blickman JG, Dacher JN, Darge K, Lobo ML, Willi U. Imaging recommendations in paediatric uroradiology. Minutes of the ESPR uroradiology task force session on childhood obstructive uropathy, high-grade fetal hydronephrosis, childhood haematuria, and urolithiasis in childhood. ESPR Annual Congress, Edinburgh, UK, June 2008. Pediatr Radiol 2009; 39: 891-8.









