Enuresis
Mike O'Brien
Departamento de Urología, Royal Children's Hospital, Melbourne, Australia
Traducido y editado desde el original al español | Enlace a la versión en inglés
Dr. Juan Carlos Prietoa, Dr. Ricardo Antonio Arceo Olaizb
aMethodist Children's Hospital, San Antonio, Texas; Children's Hospital of San Antonio, San Antonio, Texas
bHospital Shriners para Niños Ciudad de México, México
Se ha dicho que la enuresis nocturna o enuresis es la condición infantil más común que afecta a un estimado de 5 a 7,000,000 niños estadounidenses mayores de 6 años (1). Existen múltiples publicaciones sobre tasas de prevalencia en todo el mundo que muestran una consistencia notable. Entre los niños australianos, de 5 a 12 años de edad, la prevalencia general de cualquier enuresis nocturna fue del 18,9% y del 15% para la enuresis aislada (2). La mayoría de los niños se vieron afectados menos de una vez al mes. La enuresis marcada, definida como al menos semanalmente, ocurrió en el 5%, con un predominio masculino. El Estudio Longitudinal Avon de Padres e Hijos (ALSPC) encuestó a 11,251, de los cuales 8,269 (73.5%) respondieron con 15.5% de los niños de 7.5 años mojando la cama, 83% haciéndolo a lo sumo una vez por semana (3). Utilizaron el Manual Diagnóstico y Estadístico de los Trastornos Mentales, cuarta edición (DSM IV), el cual define la enuresis nocturna como la fuga involuntaria de orina durante el sueño, con una frecuencia de al menos dos veces por semana en niños mayores de 5 años. En Hong Kong, la enuresis nocturna, definida como al menos una noche húmeda cada 3 meses, afecta al 16% de los niños de 5 años, al 10% de los niños de 7 años y al 2,6% de los niños de 10 años (4). La enuresis nocturna (no definida) se ha informado en el 5,6% de los niños coreanos de 5 a 13 años (5).
A pesar de estas diferencias en las definiciones, las tasas de prevalencia son notablemente similares. Si bien enfocarse en estas diferencias en las definiciones puede parecer pretencioso, existen implicaciones negativas para la comparación y el metanálisis (6). Esto llevó a la International
Continence Society en 1973 a establecer un comité para la estandarización de la terminología de la función del tracto urinario inferior. Esto condujo en 1998 a la publicación de estándares y definiciones de síntomas y disfunción del tracto urinario inferior en niños (7). Los avances en la investigación y la comprensión de la fisiopatología de la enuresis llevaron a la necesidad de proporcionar "directrices firmes e inequívocas para la terminología de la función del tracto urinario inferior y el mal funcionamiento en la infancia" por la International Children's Continence Society (8). Su recomendación es que el término 'enuresis' esté reservado para cualquier tipo de incontinencia urinaria intermitente que ocurra durante el sueño. El término "nocturno" se puede usar si se desea, pero no es necesario, ya que el término "enuresis diurna" ahora está obsoleto, y ha sido reemplazado por la "incontinencia diurna" más simple y descriptiva.
Los enuréticos todavía componen una población muy heterogénea de pacientes. Los enuréticos primarios se definen como aquellos que nunca han tenido un período prolongado de sequedad nocturna de 6 meses o más de duración. Se considera que aquellos que tienen enuresis secundaria sí han logrado estar secos este periodo ya descrito. Esta distinción es probablemente de poca relevancia clínica en pacientes con enuresis nocturna monosintomática (9). La enuresis nocturna monosintomática describe a aquellos pacientes con enuresis nocturna en ausencia de CUALQUIER otro síntoma del tracto urinario inferior, es decir, aumento o disminución de la frecuencia de la micción, incontinencia urinaria diurna, urgencia, pujo, chorro urinario débil, intermitencia, maniobras de posponer la micción, una sensación de micción incompleta, goteo postmiccional y dolor genital o del tracto urinario inferior. La combinación de cualquiera de estos síntomas y la enuresis define la enuresis como no sintomática. El resto de este capítulo tratará sobre la enuresis monosintomática.
Genética / Etiología
El proyecto ALSPC informó que la razón de probabilidades para un niño que desarrolla una enuresis nocturna grave (definida como 2 o más episodios por semana) fue 3.63 veces mayor si existía un historial materno de enuresis y 1.85 veces mayor con un historial paterno (10). Cuando ambos padres tienen un historial de enuresis nocturna, hay un 77% de probabilidades de que la descendencia desarrolle enuresis (11). Se sugiere que los niños con enuresis "familiar" pueden tener una variante más refractaria con más síntomas / signos de enuresis mixta en lugar de enuresis monosintomática (12). La enuresis se ha relacionado a través de estudios de segregación y enlace con varios cromosomas, incluidos 8q, 12q, 13q y 22q. En un gran estudio realizado por Loeys et al, que examinó a 32 familias con 2 a 4 generaciones de enuréticos, encontraron vínculos con los cromosomas 22q11, 13q13-14 (ENUR1) y 12q con heterogeneidad genética y sintomática / fenotípica marcada (13). Varias familias tenían vínculos con más de un locus, lo que sugiere un modo de herencia poligénico. El análisis de segregación sugiere que el modo de herencia más común es autosómico dominante con alta penetrancia (14). Es importante comprender que ENUR1 o el 'gen de enuresis' no se han identificado, sino que se ha demostrado que algunos pacientes con enuresis familiar heredaron dos marcadores específicos de microsatélites 13q13 y 13q14.2 y el gen ENUR1 está codificado en algún lugar de los 5,000,000 nucleótidos entre estos dos marcadores. Sin embargo, incluso en familias numerosas con enuresis hereditaria existe una marcada heterogeneidad dentro y entre las familias con respecto al patrón fenotípico de enuresis, es decir, primaria / secundaria, monosintomática / no monosintomática (15). Sin embargo, sí encontraron una correlación más fuerte dentro de las familias en términos de poliuria nocturna y volúmenes anulados durante el día.
Los estudios de gemelos brindan un fuerte apoyo para la modificación ambiental de una predisposición genética en la etiología de la enuresis. En 1971, Bakwin informó que 338 parejas de gemelos del mismo sexo encontraron un 68% de concordancia para la enuresis en gemelos monocigóticos y un 36% de concordancia en gemelos dicigóticos. En un estudio basado en una población finlandesa mucho más grande, la tasa de concordancia para la enuresis entre los gemelos monocigóticos fue del 46% en comparación con el 19% para los gemelos dicigóticos (16).
Fisiología / fisiopatología
En 2000, Butler y Holland propusieron "El modelo de los tres sistemas" para facilitar nuestra comprensión de la patogenia de la enuresis y para alentar intervenciones terapéuticas más dirigidas y enfocadas (17). Propusieron que la enuresis era el resultado final de la disfunción en uno o más de los siguientes tres "sistemas": i) la variación diurna normal en la liberación de vasopresina durante el sueño, ii) hiperactividad del detrusor, iii) mecanismos normales de sueño / activación. Este modelo sigue teniendo una gran validez en la actualidad, aunque al leer la literatura es evidente que las subespecialidades individuales ponen mayor énfasis en los diferentes elementos. Aunque con nuestra mejor comprensión, los tres sistemas han evolucionado hacia: i) poliuria nocturna relativa, ii) disfunción vesical nocturna, iii) retraso del desarrollo neurológico.
Poliuria nocturna
Una comprensión de la fisiología renal, que se ha incrementado enormemente en los últimos veinte años, es fundamental para comprender la fisiopatología de la enuresis y las posibles opciones terapéuticas disponibles.
El riñón tiene la tarea de mantener la homeostasis del líquido extracelular dentro de un rango muy estrecho de 280-295mOsm / kg y debe hacerlo en circunstancias que varían de un día a otro y de una hora a otra dentro de ese día. Lo hace a través de una combinación de excreción pasiva o filtración y secreción activa. El riñón adulto promedio filtra 150-180l por día, absorbiendo la gran mayoría, 90%, en el túbulo contorneado proximal y el asa de Henle. El 10% restante pasa a los túbulos distales / colectores donde se reabsorben cantidades variables de sal y agua bajo la influencia de la aldosterona y la vasopresina, respectivamente. El volumen de orina está en gran parte bajo el control de la vasopresina, que aumenta la reabsorción de agua en los túbulos colectores. El volumen de orina producido también está influenciado por la carga de soluto.
La vasopresina se libera en respuesta a un aumento en la osmolalidad plasmática detectada por osmoreceptores en el hipotálamo. Su mecanismo de acción a nivel renal se mantuvo como un misterio hasta que Agre et en 1992 describió un canal de agua que llamarían Acuaporina (19). Estas proteínas transmembrana en forma monomérica crean un poro transmembrana que se asemeja a un reloj de arena. In situ ellos
se unen para formar tetrameros con un ~ 3Å a través del cual una sola molécula de agua de ~ 2.8Å puede pasar a una velocidad de 3 x 109 moléculas de agua por monómero por segundo (20). Acuaporina 1 (AQP1) se expresa de forma constitutiva y es responsable de la mayoría de la reabsorción renal de agua que se produce en el túbulo proximal y el asa de Henle. La acuaporina 2 es la principal acuaporina regulada por vasopresina. Sus niveles de expresión en las membranas apicales del conducto colector están fuertemente regulados por la vasopresina, que se une al receptor V2 en la superficie celular y desencadena la expresión exocítica de AQP2 desde las vesículas dentro de la célula hasta la superficie apical. La eliminación de vasopresina resulta en la endocitosis (reciclaje) de AQP de nuevo en vesículas intracelulares. AQP3 y AQP4, situadas en las membranas basales y laterales, Son responsables de la liberación de agua intracelular de nuevo en la circulación. Tan significativo fue el descubrimiento realizado por Agre que en 2003 recibió el Premio Nobel de Química, que compartió con Roderick MacKinnon, quien descubrió los canales iónicos (http://www.nobelprize.org/nobel_prizes/chemistry/laureates/2003/public.htm l ).
Desde hace tiempo se sabe que en el estado normal producimos más orina durante el día que durante la noche. Roberts en 1860 observó que en la orina, se excretaba 4,5 veces más agua por día que por noche y el doble de "constituyentes sólidos". Ésta es la razón por la cual el individuo promedio puede pasar de 2.5 a 4 horas durante el día entre vacíos, pero puede abstenerse de hacerlo hasta 8 horas durante la noche. Poulton en 1952, publicó sobre el volumen de orina producido por 100 niños enuréticos y 18 controles, y observó que había un ritmo diurno de producción de orina en ambos, pero que estaba más atenuado en el grupo enurético (21). Descubrió que la proporción de la producción de orina entre el día y la noche era de 1.8 o más en el grupo de control y menor que en el 69% del grupo sintomático, con algunos tan bajos como 1.0. Fue él quien acuñó el término p_oliuria nocturna relativa_.
La investigación sobre este fenómeno permaneció inactiva hasta el trabajo seminal de Rittig et al en Dinamarca, quien demostró muy elegantemente (en un entorno muy bien controlado) un ritmo circadiano diurno marcadamente marcado de los niveles plasmáticos de vasopresina en niños enuréticos en comparación con controles sanos (22). El nivel plasmático nocturno de vasopresina fue significativamente menor en los niños afectados. De manera similar, encontraron que ambos grupos produjeron un volumen similar de orina en un período de 24 horas en niños normales sanos que demostraron una reducción marcada en la producción nocturna de orina reducida en casi un 66%, mientras que los niños enuréticos no demostraron tal reducción. También demostraron un ritmo circadiano a la osmolalidad de la orina que era recíproco al volumen de orina en controles sanos y la ausencia de dicho ritmo en los enuréticos.
¿Por qué es que el tratamiento con desmopresina (dDAVP) inducirá una respuesta en más del 70% con una reducción en las noches húmedas, pero solo cura el 24,5%? ¿Por qué no todos los enuréticos con poliuria nocturna responden a la desmopresina? Al menos en parte, esto puede deberse a una mayor carga de solutos en la noche, que independientemente tiene la capacidad de aumentar el volumen de orina. Esto se ve corroborado por el hecho de que, al menos en parte, se cree que los antidepresivos tricíclicos reducen la enuresis al disminuir la excreción nocturna de solutos (23). Nuevamente, Rittig et al demostraron muy elegantemente que en un subgrupo de enuréticos su poliuria nocturna se asoció con una natriuresis significativa con una ausencia asociada de aumento nocturno en la angiotensina II o la aldosterona. Aceto et al encontraron una asociación similar entre la enuresis, poliuria nocturna y excreción nocturna de sodio (24). Ese mismo grupo también encontró una asociación entre poliuria nocturna e hipercalciuria absorbente. A pesar del sesgo de selección de la derivación a un nefrólogo pediátrico del centro de referencia terciario en Gante, Bélgica encontró hipercalciuria en el 12% de los niños enuréticos, que probablemente reflejaban la ingesta dietética en lugar de la hipercalciuria primaria, como la observada en el trabajo de Caione et al de Italia. (25). Valenti et al encontraron que los niveles de Acuaporina 2 en la orina se correlacionaban bien con la gravedad de la enuresis (26). En niños normales, la proporción de excreción urinaria de AQP2 de día a noche fue de 0.6 en comparación con 1.2 en enuréticos. Además, encontraron que los niveles bajos de vasopresina y la hipercalciuria se asociaron de forma independiente con un aumento de dos veces en el cociente AQP urinario día / noche y que los niveles bajos de vasopresina cuando se asociaron con hipercalciuria dieron como resultado un aumento de tres veces. No todos creen que la hipercalciuria sea causante de enuresis (27). A pesar de sus dudas, se ha realizado un trabajo reciente para sugerir que la hipercalciuria que actúa a través del receptor de detección de calcio apical interfiere con la función de la vasopresina, lo que resulta en una mayor excreción urinaria de AQP y diuresis (28).
Otras hormonas que se han investigado incluyen el péptido natriurético auricular (sin asociación clara) y la prostaglandina E2, que presenta una clara variación diurna en niños normales con una caída del 30% durante la noche (29,30). Al observar más de cerca a la PGE2, que es un antagonista conocido de la vasopresina, el grupo danés encontró nuevamente niveles significativamente elevados de PGE2 en orina en enuréticos con poliuria nocturna, refractarios a la terapia con desmopresina, en comparación con controles sanos, enuréticos no poliúricos y enuréticos que tenían noches secas (31).
Es evidente que una gran proporción de enuréticos tienen poliuria nocturna. Sin embargo, no todos estos se deben a una deficiencia de vasopresina. Además, todas las personas con poliuria nocturna tendrán enuresis, pueden tener nocturia, es decir, de despertar para orinar.
Disfunción vesical nocturna
Ya en 1878, Ruddock sintió que la causa de la enuresis puede estar en una vejiga hipertrófica con mayor contractilidad (32). Existe una asociación bien establecida entre la enuresis y la disfunción vesical diurna con aproximadamente el 20% de los enuréticos que también presentan síntomas diurnos, es decir, enuresis no monosintomática. Para estos pacientes, parece lógico que al menos en parte la disfunción de la vejiga contribuya a su enuresis. En los enuréticos monosintomáticos, sin embargo, se ha entendido tradicionalmente que su función subyacente de vejiga era normal. La videourodinámica llevada a cabo en pacientes enuréticos confirmó esta suposición al no mostrar una mayor tasa de hiperactividad de detrusor en comparación con controles sanos, cuando los pacientes estaban despiertos. En 1989, Watanabe informó sus resultados con EEG combinado durante la noche y cistometría en 204 enuréticos y 3 controles sanos (33). Según su trabajo, pudieron dividir a los pacientes enuréticos en tres grupos.
Tipo I (61%): respuesta similar de la vejiga al llenado como controles sanos, sin embargo, a medida que se acercaba la capacidad de la vejiga y se observaba la primera contracción del detrusor en la cistometría, la etapa del sueño cambió, pero no hasta el punto de despertar antes de que ocurriera la enuresis.
Tipo IIa (11%): hallazgos similares mientras dormían como sujetos normales, sin embargo, ni la primera contracción del detrusor cuando se acerca la capacidad de la vejiga ni la enuresis en sí se asociaron con un cambio en el EEG.
Tipo IIb (28%): hallazgos similares en el EEG, pero cuando los pacientes entraron en el sueño profundo, la cistometría demostró contracciones no inhibidas continuas del detrusor (no se veían cuando estaban despiertos) y se produjo enuresis sin un cambio notable en el EEG.
Estos subtipos y porcentajes fraccionarios fueron confirmados por el mismo grupo con una serie mayor de 826 pacientes en 1994 (34). No encontraron ninguna diferencia en la capacidad funcional de la vejiga entre los enuréticos y los no enuréticos después de los 7 años de edad.
Yeung et al en Hong Kong utilizaron una combinación de cistometría de llenado fisiológico por día y cistometría simultánea y EEG durante el sueño en 95 pacientes con enuresis refractaria al tratamiento con desmopresina y / o terapia de alarma (35). Pudieron distinguir entre dos subgrupos en esta población. El grupo A (35%) tenía una función vesical normal durante el día, pero demostró una hiperactividad significativa del detrusor y una marcada reducción en la capacidad funcional de la vejiga después de quedarse dormido. El grupo B (65%) tuvo un patrón similar cuando estaba dormido, pero también una urodinamia diurna anormal que no se detectó previamente. Ellos enfatizan la importancia de una historia detallada y una tabla de volumen de frecuencia para buscar aquellos enuréticos que han adaptado inconscientemente su comportamiento durante el día para mitigar los síntomas de la disfunción de la vejiga (36).
Otra evidencia de la interacción entre los tres sistemas de Butler y el modelo de Hollands proviene del hallazgo de que el uso del sistema de alarma y del timbre, pensado para abordar las anomalías de la excitación o la vigilia, de hecho, también altera la capacidad de la vejiga nocturna. Oredesson demostró un aumento en la capacidad de la vejiga nocturna de una media de 270 ml de tratamiento de pre-alarma a 370 ml después de 6 semanas de terapia de alarma, en 10 de los 18 pacientes que lograron estar secos (38). Incluso en los 8/18 que no se secaron, demostraron un aumento de la capacidad de la vejiga nocturna de 235 a 294 ml después de 6 semanas de tratamiento. Ambos grupos tenían capacidades diurnas aceptables de 345 ml y 315 ml, respectivamente, antes del inicio del tratamiento, lo que sugiere una enuresis monosintomática. Norgaard et demostraron contracciones del detrusor en el 50% de los enuréticos durante la cistometría del sueño, que podrían incrementarse hasta el 100% mediante diuresis forzada (39). Esto apoya el papel de la interacción entre los factores que pueden causar poliuria nocturna y la hiperactividad del detrusor nocturno.
Retraso del desarrollo neurológico
En 1879, Powers describió los experimentos llevados a cabo por Goltz, quien mientras limpiaba perros con médulas espinales seccionadas notó que tocar el perineo con una esponja húmeda inducía la micción y lo atribuía a una liberación de "influencias mentales superiores" similar a cuando dormía (32).
Así como es importante tener una comprensión de los mecanismos renales que controlan el volumen de la orina, el urólogo también debe entender el control neural de la función de la vejiga. En los últimos veinte años, nuestra comprensión del control neuroanatómico y neurofisiológico de la función de la vejiga (almacenamiento y micción) ha aumentado enormemente. Esta función biológica aparentemente simple requiere una integración muy compleja de los sistemas nervioso autónomo (simpático y parasimpático) y somático para controlar tanto la musculatura lisa como la estriada. Todo esto sucede bajo el control y la supervisión de estructuras cerebrales superiores que reflejan un comportamiento adquirido o aprendido. Incluso ahora todavía hay mucho que aprender con modelos aún diferentes del control de la micción. Una descripción detallada sobre este tema va más allá del alcance de este texto y el lector es referido a los trabajos de DeGroat, Hostege y Blok (40, 41, 42).
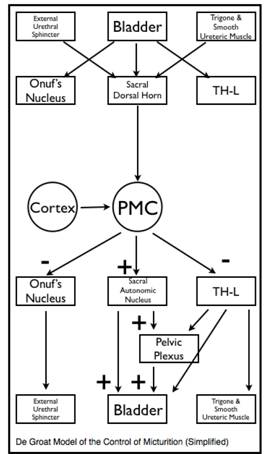 Figura 1
Figura 1
A diferencia de muchos animales, los humanos al nacer son muy inmaduros en su desarrollo tanto físico como mental / neurológico (43). Ahora parece que 5/6 del crecimiento del cerebro humano se produce después del parto y la mielinización rápida no se completa hasta aproximadamente la edad de 3-4 años. Esto explica el logro gradual y progresivo de los hitos del desarrollo, como sentarse a 7 meses, gateando a 9 meses, caminando a 12 meses y las tasas de progreso más lentas para funciones más altas como hablar, comprender, socializar, etc. Sabemos que el control de la vejiga es un fenómeno adquirido que progresa del vaciado automático o reflexivo de la vejiga de un neonato, a la capacidad volitiva de abstenerse e iniciar el vaciado de la vejiga bajo demanda que sigue al entrenamiento exitoso del baño. Koff argumenta que trazar una línea en la arena y decir que más allá de ese tiempo una ocurrencia normal previamente aceptada es ahora un proceso patológico en lugar de una simple reflexión de desarrollo tardío es contraintuitivo (44). Sobre la base de gran parte de la evidencia ya presentada, propone la existencia de un retraso de desarrollo dual en su SNC.
Retraso de desarrollo eferente: un fallo del SNC para suprimir el arco reflejo de micción mientras el paciente está dormido, también debe asociarse con un fallo para despertarse.
En 1989, Javelin informó sobre el desarrollo neurológico de 156 enuréticos y 170 controles, niños de 7 años, a los cuales observaron su desarrollo e historias perinatales y aplicaron una prueba de deterioro motor (45). Él, como otros, encontró más torpeza motora fina y gruesa en los niños enuréticos. Los niños enuréticos también tienen tasas de crecimiento más lentas, lo que sugiere que la enuresis aislada se asoció con un retraso evidente en el desarrollo. Además, esos pacientes tuvieron la mayor influencia genética, lo que sugiere que el retraso en el desarrollo fue de origen genético. Los eventos perinatales no tuvieron una asociación significativa con la enuresis monosintomática, pero pequeños para edad gestacional, la asfixia y otras lesiones neurológicas durante el período neonatal se asociaron con un mayor riesgo de desarrollar enuresis no sintomática. Otros también han encontrado evidencia de retraso neuromotor generalizado y disfunción específica del tronco cerebral en enuréticos (46). Ese mismo grupo también encontró evidencia de retraso en la maduración de la corteza motora del cerebro (47). Ornitz et al utilizaron muy hábilmente la inhibición prepulso (IBP) de un reflejo de sobresalto para modelar la inhibición refleja de la contracción de la vejiga durante el llenado mediado por el núcleo tegmental pedúnculopontino a través de la región L del centro de micción pontino (48). En resumen, el reflejo de inhibición prepulso es un embotamiento del reflejo de sobresalto normal en respuesta a una visión auditiva, visual o 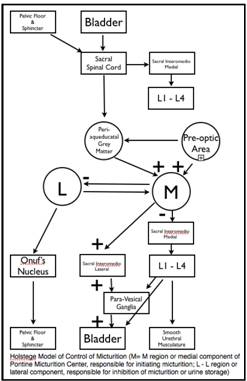 estímulo táctil por sensibilización previa con un estímulo mucho más débil 120 mseg antes. En comparación con el control de los niños, los enuréticos tienen una respuesta PPI deficiente. Es interesante que esta deficiencia se mantiene incluso después de que la enuresis se haya resuelto, lo que sugiere un posible rasgo hereditario que predispone a la enuresis en lugar de un retraso del desarrollo per se (49).
estímulo táctil por sensibilización previa con un estímulo mucho más débil 120 mseg antes. En comparación con el control de los niños, los enuréticos tienen una respuesta PPI deficiente. Es interesante que esta deficiencia se mantiene incluso después de que la enuresis se haya resuelto, lo que sugiere un posible rasgo hereditario que predispone a la enuresis en lugar de un retraso del desarrollo per se (49).

Figura 2
Cuando se les pregunta a las familias qué creen que es la causa de la enuresis, casi universalmente apuntan a la profundidad del sueño del paciente y su incapacidad para despertarlo. Sin embargo, numerosos estudios sobre el sueño han demostrado una arquitectura normal del sueño y que los episodios enuréticos ocurren durante todas las etapas del sueño. Es su viabilidad lo que se deteriora. Wolfish demostró que los varones enuréticos eran más difíciles de despertar que los controles emparejados por edad, con el 9.3% de los primeros y el 39.7% de los últimos respondiendo a estímulos acústicos de hasta 120dB (50). Esto es consistente con la experiencia de los padres que 'levantan' a sus hijos para orinar durante la noche, generalmente señalando que pueden hacerlo sin que parezca que están completamente despiertos. Además, la terapia de alarma a menudo se abandona temprano debido a una falla en despertar al paciente a pesar de despertar a todos los demás miembros del hogar. Un informe reciente que utiliza una tecnología diferente (un Actigraph, que documenta el movimiento) llevado a cabo en el entorno del hogar del paciente en lugar del hospital, sugiere que los enuréticos no tienen una arquitectura de sueño normal como se indicó anteriormente, sino que tienen un sueño más fragmentado con más despertares nocturnos y más movimiento durante el sueño (51). Esto no es incompatible con el trabajo anterior, ya que una mayor perturbación del sueño puede resultar en una mayor privación del sueño y, por lo tanto, mayores umbrales de activación.
Ha habido múltiples informes contradictorios de asociaciones entre la enuresis y otras parasomnias, como caminar dormido, hablar dormido, pesadillas, etc. Durante mucho tiempo se ha sostenido la creencia de una asociación entre la obstrucción de la vía aérea superior y la enuresis. A fines de 1800, una asociación de respiración bucal y enuresis se atribuyó al envenenamiento por ácido carbónico (32). Más recientemente, un informe de Turquía examinó a 321 niños que se sometieron a una adenoamigdalectomía, de los cuales 111 presentaban enuresis antes de la operación (52). Setenta y cuatro de los enuréticos estaban disponibles para la evaluación después de la operación, de los cuales 47 ya no se quejaban de la enuresis y 3 tenían una frecuencia reducida. Informan una tasa de curación del 63% que, incluso con la intención a tratar, el análisis del 111 original aún sería del 46%.
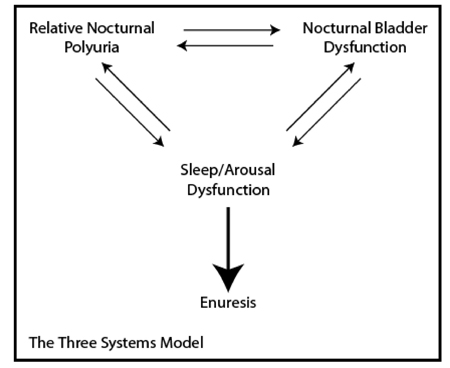
Figura 3
En última instancia, la enuresis se produce porque el paciente no logra despertar para anular una vez que el volumen de orina en la vejiga se acerca o supera su capacidad para contenerla.
Diagnóstico
El diagnóstico de enuresis es fundamentalmente clínico, y se basa casi en su totalidad en la historia obtenida del paciente y del padre. Lo que es crucial durante la historia clínica es, en primer lugar, excluir otras formas de incontinencia urinaria, ya sea una incontinencia mixta de día y de noche que sugiera una disfunción vesical subyacente, una incontinencia continua que sugiera anomalías estructurales o anatómicas o una enuresis secundaria más sugerente de otras causas médicas o psicológicas (53).
El historial realizado debe ser extenso y exhaustivo y abarcar todas las áreas descritas anteriormente. La naturaleza de la incontinencia urinaria (día o noche), la frecuencia de aparición (relacionada con el pronóstico), la gravedad y el momento (puede influir en la selección del tratamiento), la duración de los síntomas (primaria o secundaria), la presencia de otros síntomas diurnos sugestivos de disfunción vesical (frecuencia, urgencia, maniobras para retrasar la micción), antecedentes de infecciones del tracto urinario, ingesta dietética (tiempo, naturaleza de los alimentos / líquidos, etc.), hábito intestinal que incluye incontinencia fecal, problemas de comportamiento (TDAH, dificultades de aprendizaje, trastornos del sueño / parasomnias) , ronquidos o apnea del sueño. Es importante comprender el historial médico pasado, incluidos los eventos prenatales y perinatales, así como el historial de desarrollo. Antecedentes familiares de enuresis ya que apunta al pronóstico. La historia social como eventos múltiples de la vida (p. Ej., nuevo hermano, separación de los padres, etc.) puede indicar comorbilidad psicológica.
Como estos pacientes a menudo son retraídos e introvertidos, el examen físico (al menos en la consulta inicial) se puede mantener con seguridad en un mínimo de mediciones antropométricas (para excluir parcialmente el retraso del desarrollo), presión arterial y análisis de orina (para excluir patología renal), palpación abdominal ( para evidencia de carga fecal si la historia lo sugiere). En ausencia de características sugestivas en la historia, el examen genital / perineal rara vez está indicado, ni un examen neurológico detallado (más allá de ver al paciente entrar a la sala de exploración) (54).
Investigaciones
Pocas investigaciones, si las hay, son necesarias en la enuresis monosintomática más allá del análisis de orina. Si bien no es estrictamente una investigación, la herramienta de investigación más útil es un diario detallado de frecuencia / evacuación o eliminación. Puede ayudar a dirigir la terapia documentando la poliuria nocturna o desenmascarando la sintomatología diurna.
Tratamiento
Un estudio encontró que entre el 23 y el 36 por ciento de los padres habían usado el castigo como su principal medio para lidiar con orinarse en la cama (55).
"Sabía que mojar la cama era a) malvado y b) fuera de mi control … Por lo tanto, era posible pecar sin saber que lo cometiste, sin querer hacerlo, y sin poder evitarlo … La doble paliza fue un punto de inflexión porque me trajo a la memoria por primera vez la dureza del entorno en el que me habían lanzado … Tenía una convicción de pecado y locura y debilidad, como no recuerdo haber tenido nunca antes ".
Los ensayos recolectados, periodismo y cartas de George Orwell. Vol. IV. Delante de tu nariz, 1945-1950. Nueva York: Penguin Books, 1970. (56)
El tratamiento médico moderno de la enuresis nocturna ha recorrido un largo camino desde el castigo o el afeitado del testículo de la liebre hasta el vino fragante para beber. En 1545, el peine de un gallo o las piedras de un erizo se utilizaron de manera similar (32).
Los requisitos previos esenciales para el tratamiento exitoso de la enuresis nocturna son un niño motivado, padres comprensivos y cooperadores, con expectativas realistas, y un terapeuta entusiasta, interesado e informado (57). Para la enuresis nocturna primaria, el terapeuta puede ser el médico de familia, el enfermero clínico, el fisioterapeuta de continencia, el pediatra o el urólogo pediatra.
Antes de comenzar cualquier intervención médica, son apropiadas las modificaciones de comportamiento simples basadas en la historia del paciente y el diario miccional. Esto a menudo se conoce como uroterapia. En su mayor parte, éstas son sugerencias de sentido común basadas en lo que se ha escrito anteriormente. Los pacientes deben tener un hábito regular de micción durante el día y, obviamente, lo último en la noche antes de dormir. Deben consumir un volumen adecuado, del tipo correcto de líquidos, por ejemplo, agua en lugar de refrescos, en el momento adecuado, es decir, beber la mayoría al comienzo del día y la tarde y limitar los líquidos a la hora de acostarse a solo el requerido para calmar la sed. Deben comer con sensatez, lo suficiente para evitar o tratar el estreñimiento y deben abstenerse, en la medida de lo posible, de comidas pesadas llenas de calcio y sal cerca de la hora de acostarse. Esto es difícil de llevar a cabo, ya que en muchas familias occidentales la comida principal del día se consume por la tarde cerca de la hora de dormir, en enuréticos entre 7 y 10 años de edad.
Aunque no hay evidencia directa para respaldar estas simples medidas clínicas en la enuresis monosintomática, implican poca carga adicional y hay evidencia circunstancial de que el estreñimiento, por ejemplo, es casi cinco veces más común en enuréticos que en no enuréticos (58).
Con estas medidas simples e intuitivas bien establecidas, debe considerarse la terapia complementaria.
Para una revisión exhaustiva del manejo de la enuresis nocturna en niños y adolescentes, el lector debe consultar las directrices del Instituto Nacional de Salud y Excelencia Clínica (NICE) para la gestión de la enuresis nocturna, publicadas en octubre de 2010 por el NHS en el Reino Unido (http: //www.nice.org.uk/nicemedia/live/13246/51367/51367.pdf). Nos referiremos aquí a las diversas opciones de tratamiento disponibles que intentan lógicamente abordar las anomalías patológicas subyacentes en los tres sistemas descritos anteriormente. Algunos autores han sugerido subdividir la enuresis nocturna en subcategorías dependientes de desmopresina y depender de detrusor.
Desmopresina
El tratamiento con desmopresina tiene sus orígenes en el uso de polvo pituitario, y posteriormente de pituitaria posterior, para reducir el volumen urinario. El primer reporte de polvo pituitario para tratar diabetes insípida fue en 1924; y 1925 se utilizó por primera para tratar enuresis nocturna en niños. No fue sino hasta 1955 que un estudio cruzado doble ciego de Di-sipidin (polvo de pituitaria posterior) versus placebo fue llevado a cabo por Marson en Leeds (59). Él encontró una importante reducción en la incidencia de enuresis durante el tratamiento con el polvo en 4 adolescentes seleccionados.

Figura 4
Hoy en día s (Figura 3) e usa desmopresina, un análogo sintético de la vasopresina, disponible desde 1980. La desmopresina, o dDAVP, se crea al desaminar el residuo de cisteína (que prolonga su actividad) en un extremo de la vasopresina y al reemplazar la L-arginina con D-arginina (que reduce la actividad del vasopresor). De este modo, dDAVP se convierte en un potente antidiurético con una actividad vasopresora reducida y una vida media prolongada de 1,5 a 3,5 horas en comparación con los 12 minutos de la vasopresina (60). El tiempo para la actividad biológica máxima después de la ingestión es de aproximadamente 60 minutos (61). Su inicio de acción rápido significa que a menudo se recomienda cuando se necesita una respuesta rápida (como ir a campamentos durante la noche, dormir fuera de casa, etc.).
Hay pruebas claras de que, en comparación con el placebo, la desmopresina reduce el mojar la cama de una a dos noches (62). Las personas que reciben desmopresina tienen casi el doble de probabilidades de curarse con las que reciben placebo (que se define como lograr 14 noches secas consecutivas). La tasa de éxito a corto plazo para el tratamiento con desmopresina es del 69% (rango 32-100%), con tasas de éxito a largo plazo de 45,7% (rango 7-78%) (63). Con una mejor selección de pacientes a través del uso de pruebas diagnósticas invasivas menores como la cistouretrografía miccional, la cistometría y la videocistometría, las tasas de éxito a corto plazo mejoran a 84% (47-97.2%) y a largo plazo hasta el 78,5%. Éste es probablemente el resultado si se seleccionan pacientes con formas leves de enuresis no monosintomática. Una retirada gradual de la desmopresina está asociada con un beneficio prolongado mayor; con 57% teniendo menos de 2 noches húmedas por mes en los que lo suspendieron abruptamente, comparado con un 80% en aquellos que lo retiraron de manera gradual (64).
La desmopresina viene en una variedad de preparaciones a base de intravenosas, gotas nasales, aerosol nasal, tableta oral y, más recientemente, una nueva preparación oral que se derrite rápidamente (61). Aproximadamente el 1% de la desmopresina administrada por vía oral aparece en la sangre y está biológicamente disponible, en comparación con el 11% de dDAVP intranasal (64). La biodisponibilidad mejorada del aerosol nasal se ve mitigada por 1) el aumento del riesgo de efectos secundarios, de gravedad variable desde la epistaxis hasta la hiponatremia (63); 2) variabilidad en la absorción y eficacia durante enfermedades nasales intercurrentes como infección del tracto respiratorio superior, alergia y congestión nasal, etc. Para compensar la biodisponibilidad de la administración oral, las tabletas tienden a tener una dosis diez veces mayor de dDAVP. Sin embargo, existe evidencia de que la interacción con los alimentos en el tracto GI afecta la biodisponibilidad de la dDAVP y posiblemente explica alguna inconsistencia del efecto en los pacientes que responden con desmopresina. La recientemente lanzada desmopresina Melt presenta el dDAVP como un liofilizado oral que se disuelve inmediatamente en la boca, sin la necesidad de agua, lo que hace que la presentación sea más aceptable y agradable para los niños (61). La formulación en estado fundido, así como una absorción más confiable, tienen una bioeficacia mejorada y predecible: una dosis de 60 mcgs de masa fundida tiene el efecto biológico equivalente a 100 mcgs de comprimido. Dicho esto, no se ha demostrado ninguna diferencia significativa en el efecto clínico entre las tabletas y las masas fundidas sublinguales (63).
Parece que hay una mayor probabilidad de éxito con una mayor duración del tratamiento, por ejemplo, 3 meses. La terapia prolongada con desmopresina ha demostrado ser eficaz y segura (66).
Por lo tanto, las recomendaciones actuales para el uso de desmopresina son que se puede ofrecer a niños mayores de 7 años y se puede considerar para aquellos entre 5 y 7 años. Es apropiado cuando se necesita un tratamiento de inicio rápido o de corta duración o en aquellos en los que la terapia de alarma no es apropiada (se moja <2 noches / semana) o que han fallado a la terapia de alarma. No tiene ningún papel en el manejo de la incontinencia diurna aislada, pero la enuresis no monosintomática no es una contraindicación para su uso (junto con el manejo de los síntomas diurnos). Se debe comenzar con una dosis baja de 120 mcgs para Melt o de 200 mcgs para tableta y considerar duplicar la dosis después de 2 semanas en pacientes que no respondieron. Para aquellos que no respondieron después de 4 semanas (en dosis más altas), considere la posibilidad de interrumpir, reevaluar y una terapia alternativa o combinada (67).
Terapia de alarma
El precursor de la almohadilla y la campana de hoy en día fue descrito por Nye en 1881, quien colocó una esponja seca sobre el meato uretral y una esponja húmeda entre los omóplatos que conectan los dos por una batería. Mientras que la esponja uretral estaba seca, el circuito no conduciría, pero cuando se humedece con la orina "despertará" al paciente en el acto. Una repetición de una experiencia similar durante un número suficiente de veces, me inclino a pensar, debería curar al paciente. (32) La idea en ese momento era que la enuresis surgía de la excitación indebida y la disposición a contraerse de las vejigas (69). Fue para sofocar esta excitabilidad que se recetaba Belladonna. Sin embargo, se reconoció la naturaleza conductiva del sueño profundo y, por ende, de la electricidad, ser un estimulante (para tratar la profundidad del sueño), así como un sedante (para tratar la excitabilidad de la vejiga) parece ser adecuado para ambos ". Debe recordarse que aunque el término fue acuñado en el siglo XVII por William Gilbert, la electricidad realmente despegó a fines del siglo XVIII y principios del XIX, por lo que hubo muchas aplicaciones en medicina, incluida la publicación por Erb en 1882 de un Manual de Electro-Terapé__utica que recomienda la aplicación de electricidad externa e internamente a la uretra.
La terapia de alarma ha sido durante mucho tiempo el tratamiento de primera línea establecido para la enuresis. Las alarmas modernas continúan haciendo uso de la conductividad eléctrica de la orina para completar un circuito eléctrico y desencadenar un estímulo de activación, generalmente audible pero recientemente vibratorio. Los sistemas de alarma tradicionales utilizan una almohadilla grande colocada en la cama conectada a la caja de alarma. Cambios recientes en las alarmas han hecho que se utilize una pequeña tira conductora colocada en la ropa interior del paciente y conectada a una alarma corporal (p. Ej., WetAlert, Dri Sleeper Excel, Enurad 400, etc.). Algunos utilizan una combinación de sonido y vibración y pueden ser inalámbricos (por ejemplo, Malem Ultimate, PottyMD Wet Stop3, etc.). Siempre ha habido una gran selección de alarmas para elegir, con poca o ninguna característica distintiva (70).
Una revisión reciente de Cochrane sobre el uso de la terapia de alarma en el tratamiento de la enuresis revisó 56 estudios, con 3257 niños que encontraron que, en comparación con ningún tratamiento, aproximadamente dos tercios de los niños se secaron cuando utilizaban una alarma (71). Para aquellos en quienes funciona, casi la mitad permanece seca después del tratamiento. Encontraron poca evidencia para favorecer una alarma en particular sobre otra, pero hubo una sugerencia de que las alarmas que despertaron al paciente directamente en lugar de a un padre tuvieron más éxito. La terapia de alarma parece ser más efectiva con el uso prolongado.
Han habido varios intentos para complementar el éxito de la terapia de alarma que varía desde modificaciones de comportamiento adicionales, como entrenamiento de control de retención, aprendizaje excesivo, entrenamiento en cama seca, sistemas de recompensa (tablas de estrellas, etc.) o sistemas de castigo. En general esto tuvo poco o ningún valor adicional. El único con algún mérito es el sobre-aprendizaje. Esto requiere que un paciente que haya logrado 14 noches secas consecutivas desafíe su vejiga consumiendo líquidos adicionales durante la noche y continúe con la terapia de alarma hasta que se logren 14 noches secas consecutivas. Ciertamente, la adición de un aprendizaje excesivo redujo la tasa de recaída, al igual que el entrenamiento en cama seca. El aprendizaje excesivo se asoció con una tasa de recaída reducida del 49% al 25% y el entrenamiento en cama seca del 63% al 27%. El entrenamiento en cama seca, desarrollado en los años 70 para pacientes con discapacidad en el aprendizaje, incluye un programa intensivo de despertar durante la noche y un régimen punitivo de "entrenamiento limpio" si el hecho de mojar ocurre - este abordaje más bien oneroso y algo negativo, no tiene mayor atracción para este autor, al igual que alarmas que administran un choque eléctrico.
Quizás el mayor problema con la terapia de alarma es la adherencia con el tratamiento o el cumplimiento. El grupo de Gante ha demostrado un notable cumplimiento, aprox. 75%, con estrategias de comportamiento como beber y anular horarios (72). Los factores que identificaron como que tenían un impacto positivo en el cumplimiento con el manejo médico incluían la autopercepción de la apariencia, sentirse menos estresados por su condición y una actitud madura hacia la resolución de problemas. Se ha demostrado que las tasas más altas de abandono (10 a 30%) de los ensayos se asocian con intolerancia de los padres, problemas de conducta con el niño de una autoimagen negativa. Los problemas de cumplimiento no están relacionados con los efectos secundarios, ya que hay muy pocos, si es que los hay. Los días de las 'úlceras por zumbido' se han ido con la tecnología moderna.
Cuando Watanabe expuso evidencia de EEG de un cambio en el sueño de profunda a ligero, basado en los cambios de onda delta, desarrolló un sistema de alarma basado en el EEG que alertaría a una enfermera cuando el patrón de sueño cambiaba agudamente y luego la enfermera despertaría al paciente. La ventaja percibida es que el paciente fue despertado antes de que ocurriera la enuresis. Demostraron beneficios en el 55% y curaron en el 17% después de 5 a 6 noches de terapia hospitalaria (34).
Lo que aún no está claro es por qué funciona la terapia de alarma. El enfoque simplista es creer que funciona como una forma de condicionamiento aversivo, es decir, el paciente se despierta cuando la vejiga alcanza su plenitud para evitar el doloroso estímulo audible. Otros consideran que es una forma de condicionamiento operante en el sentido de que la sensación asociada con el llenado de la vejiga se asocia al despertar del sueño al vacío. Sin embargo, la mayoría de los niños que se secan mientras usan la terapia de alarma lo hacen mientras duermen toda la noche sin mojarse (65%) en lugar de despertarse para orinar (35%). Para ilustrar aún más nuestra ignorancia continua de la complejidad involucrada en la enuresis, a pesar de los niveles de comprensión ilustrados por DeGroat, Holstege, Yeung et al. hubo una publicación reciente de Schulz-Juergensen et al. Encontraron que la dDAVP administrada a niños enuréticos incrementó su reflejo de Inhibición del sobresalto prepulso hasta el nivel de los controles normales, mientras que el placebo no lo hizo (73). Esta evidencia de un papel de acción central para la desmopresina, así como su papel renal, demuestra la interacción compleja entre el sistema nervioso central y los órganos periféricos en la patogénesis de la enuresis.
Las recomendaciones actuales de tratamiento para la alarma son que debe ofrecerse como una terapia de primera línea para los enuréticos motivados que no han respondido a la modificación de la conducta o la uroterapia, que se mojan más de dos veces por semana y tienen padres o tutores que los apoyan. Si no hay signos de mejoría después de 4 semanas, el tratamiento debe interrumpirse. El tratamiento exitoso debe continuar hasta un mínimo de 14 noches secas consecutivas (67). La terapia de alarma requiere un mínimo de 6-8 semanas de uso continuo para alcanzar su efecto. Los pacientes y las familias deben revisarse quincenalmente para mantener la motivación y el cumplimiento. Es recomendable, para algunos niños, que un padre duerma en la habitación del niño al comienzo del tratamiento para ayudarlo a despertarse inmediatamente cuando suena la alarma (54).http://www.youtube.com/watch?v=cst7jPCzAs4
Medicación anticolinérgica
La medicación anticolinérgica (oxibutinina o tolterodina, por ejemplo) tiene un beneficio comprobado en pacientes con incontinencia urinaria diurna secundaria a hiperactividad del detrusor. Tiene un beneficio potencial similar en el tratamiento de niños con enuresis no monosintomática y, por lo tanto, se puede considerar de manera temprana en el tratamiento de aquellos pacientes que no responden a la uroterapia. Sin embargo, como se muestra más arriba, el 28% de los enuréticos tendrá una hiperactividad del detrusor demostrable urodinámicamente solo por la noche y, por lo tanto, el tratamiento con un medicamento anticolinérgico por la noche tiene buenos méritos. En lugar de realizar la urodinamia del sueño en todos los tratamientos con enuréticos con un anticolinérgico, se sugiere en aquellos que han fracasado o solo han respondido parcialmente a la terapia con desmopresina (57). Se recomienda que los anticolinérgicos se usen en combinación con desmopresina en vez de utilizarlos solos (67). Antes de iniciar el tratamiento anticolinérgico, se debe excluir / controlar el estreñimiento y se debe evaluar el vaciado de la vejiga para excluir los residuos postmiccionales significativos existentes, ya que éstos pueden empeorar (54). Una revisión Cochrane de 2009 no encontró pruebas del beneficio del tratamiento con oxibutinina sobre la administración de placebo (74). Sin embargo, el grupo de Watanabe en Japón ha reportado resultados exitosos en dos tercios de los enuréticos seleccionados sobre la base de la hiperactividad demostrable del detrusor nocturno. Un factor limitante significativo con la terapia con oxibutinina es la alta incidencia de efectos secundarios. Teóricamente, con una vida media de 8 a 13 horas, el alivio inmediato de la oxibutinina no debe causar efectos secundarios significativos cuando se administra por la noche. Sin embargo, Lovering et al. en 1988 no encontraron beneficios en 30 niños y encontraron efectos secundarios menores (malestar estomacal, fatiga, mareos, cefalea, sequedad de boca) en 17% (75). Una discusión más detallada de los efectos secundarios y la farmacología de la oxibutinina se proporciona en el capítulo sobre la micción disfuncional.
Dado el perfil de efectos secundarios de la oxibutinina, se probaron más agentes específicos del receptor muscarínico M3, como la tolterodina, y se determinó que tienen un papel. La tolterodina inicialmente a una dosis de 2 mg por la noche y aumentada a 4 mg después de 1-2 meses en ausencia de efectos secundarios o beneficios puede ayudar. Se ha demostrado que la tolterodina de liberación lenta a una dosis de 4 mg es significativamente mejor que el placebo cuando se usa en combinación con desmopresina, lo que resulta en una reducción del 66% en la propensión a las noches húmedas (76).
Antidepresivos tricíclicos
El uso de imipramina (Tofranil) para tratar la enuresis se describió por primera vez en 1960 (77). Tras observar la dificultad para iniciar la micción en adultos tratados por enfermedades depresivas, los psiquiatras en Melbourne, Australia probaron una dosis más baja en niños enuréticos. Desde entonces, se han utilizado muchos tricíclicos diferentes, pero la imipramina es la más común. Actúan inhibiendo la recaptura neuronal de noradrenalina y serotonina, prolongando así su efecto. También se ha demostrado que tienen propiedades anticolinérgicas, aunque es improbable que ejerzan su efecto de esta manera, ya que a menudo tienen éxito en pacientes que previamente no tuvieron tratamiento anticolinérgico. Se desconoce su mecanismo de acción exacto con múltiples posibilidades, posiblemente un efecto anticolinérgico mediado periféricamente y un relajante muscular liso, debido a un efecto simpaticomimético mediado centralmente, un efecto central o mecanismos de estimulación o estimulación de la liberación de vasopresina (57). Cualquiera que sea el mecanismo, se ha demostrado en una revisión sistemática para reducir la enuresis en aproximadaemte una noche por semana y ser curativo en el 20% de los niños (78). Sin embargo, la recaída es común al suspender el medicamento y los efectos secundarios más preocupantes pueden ser graves. Los tricíclicos además de tener efectos secundarios anticolinérgicos son cardio y hepatotóxicos y potencialmente letales. Antes de comenzar el tratamiento, debe obtenerse un ECG para excluir un intervalo QT anormal (57). Dicho esto, la gran mayoría de los efectos secundarios informados por los ensayos de imipramina fueron menores sin muertes. es extremadamente importante que el medicamento se resguarde de manera segura en el hogar y que no se exceda la dosis recomendada para evitar una sobredosis. También se recomiendan las vacaciones regulares de drogas (54). Beneficio si se ve se verá dentro de los primeros 1-2 meses. El tratamiento debe ser retirado gradualmente (67).
Se ha usado un inhibidor selectivo de la recaptación de noradrenalina, reboxetina, que mostró una respuesta en 11 de 61 niños con enuresis (79). Otros 21 (total 32 o 52%) respondieron a la combinación de reboxetina y desmopresina.
Terapia combinada
En un esfuerzo por mejorar la eficacia, la terapia combinada se está probando cada vez más. Las combinaciones incluyen desmopresina con anticolinérgico (tolterodina), desmopresina con tricíclico (reboxetina), desmopresina con terapia de alarma. Todas estas combinaciones han demostrado ser superiores a la terapia individual. El orden de la terapia adicional, es decir, la desmopresina o la alarma primero con alarma o la desmopresina agregada, no tiene impacto en el beneficio de la terapia combinada (80).
Otras terapias farmacológicas
Dada la posible implicación de la prostaglandina 2, un conocido antagonista de la vasopresina, discutido anteriormente en la patogenia de la enuresis, se han probado los inhibidores de la síntesis de prostaglandina (indometacina y diclofenaco) en niños enuréticos con un éxito limitado (81, 82). Sin embargo, una revisión Cochrane no encontró beneficios (74).
La asociación de la enuresis con una alta carga de orina en solutos ha inspirado a los ensayos de terapia diurética para la enuresis refractaria nuevamente con un cierto nivel de éxito aislado (83, 84), pero ninguno de ellos se enfrentó a los rigores de una revisión Cochrane.
Terapias alternativas
La medicina tradicional china ha afirmado tasas de éxito del 76-98% para la reducción de los episodios enuréticos después del tratamiento con acupuntura (85). En esta revisión sistemática, Bower et al identificaron 84 estudios que investigaron el uso de la acupuntura en niños para el tratamiento de la enuresis. Encontraron tasas de curación reportadas que oscilan entre 30 y 93%. Sin embargo, la mayoría de los ensayos fueron de baja calidad con una asignación al azar mínima y un pequeño intento de minimizar el sesgo. Cuando consideraron solo los 4 'mejores' estudios, encontraron que la acupuntura era superior a la medicina herbolaria china pero no a la medicina occidental antienurética estándar). Informan sobre la aplicación de IRM funcional, la cual demostró un efecto central a nivel de hipotálamo y materia gris periacueductal en respuesta a estimulación periférica y por lo tanto hipotetizar en el mecanismo de acción potencial.
Una Revisión Cochrane en 2009 que analiza terapias complementarias encontró una evidencia débil en el mejor de los casos para apoyar el uso de hipnoterapia, psicoterapia, quiropráctica, homeopatía, pero ninguna evidencia que comparara estas modalidades con el tratamiento convencional (86). La psicoterapia, la acupuntura, la hipnoterapia y la quiropráctica parecían tener algún beneficio leve mientras los pacientes recibían tratamiento, pero pocas pruebas de un beneficio persistente una vez que se suspendió el tratamiento.
Algunos investigadores han informado una asociación entre los trastornos del sueño secundarios a la apnea obstructiva del sueño y los ronquidos en adultos y niños (87). La fisiopatología teóricamente implicas un aumento del péptido natriurético. Si bien ese artículo realizó estudios de referencia que informaron la resolución de la enuresis después de una adenoamigdalectomía, muchos de ellos fueron estudios no aleatorios y retrospectivos (52). Sin embargo, un ensayo controlado prospectivo recientemente realizado en Nueva York no encontró tasas de resolución de enuresis mejoradas significativamente en niños sometidos a amigdalectomía en comparación con niños enuréticos sometidos a otras operaciones (88).
Pronóstico
Según Fergusson et al., El predictor más fuerte del resultado fue una enuresis con antecedentes familiares (89). Tener dos o más familiares de primer grado con enuresis se asoció con un retraso de 1.5 años para secarse por la noche. De manera similar y probablemente por las razones descritas anteriormente, los niños con retraso en el desarrollo son más lentos para lograr el control nocturno de la vejiga.
Resultados y complicaciones
Durante bastante tiempo, ningún tratamiento se creyó necesario o indicado, ya que la enuresis se consideró un fenómeno normal, lo que refleja diferentes tasas de logro de la continencia (90). La cifra citada a menudo de 15% de resolución espontánea o 1 posibilidad en 6 de alcanzar la sequedad nocturna por año se atribuye a Forsythe y Redmond (91). Su artículo en 1974 informó su propia serie de 1129 que habían asistido a una Clínica de Enuresis en Belfast desde 1952 a 1959 y que no habían sido tratados con una alarma eléctrica. A partir de estos pacientes y una revisión de la literatura en el momento en que publicaron tasas de 'curación espontánea' de 14% entre 5 y 9 años, 16% entre 10 y 14 años y 16% durante 15-19 años. El 3% de los pacientes seguían mojándose después de los 20 años. Cabe señalar que este estudio no se limitó a los enuréticos nocturnos monosintomáticos. La enuresis primaria sola ocurrió en 629 o el 56% de su población. Sus conclusiones se ven aún más debilitadas por el hecho de que estos 1129 pacientes "no se curaron con medicamentos ni con la operación"; todos los pacientes habían recibido tratamiento con al menos 2 fármacos con diferentes mecanismos de acción de la actividad similar a la atropina (belladona, fenobarbitona, atropina, etc.), actividad anticolinérgica (propantelina), efedrina y actividad similar a la anfetamina, sedantes (hidrocloruro de hidroxicina), diuréticos (ciclopentiazida), así como psicoterapia, modificación del comportamiento (despertarse en las noches, etc.). Sin embargo, sus tasas de resolución fueron proporcionales a otras publicadas hasta ese momento.
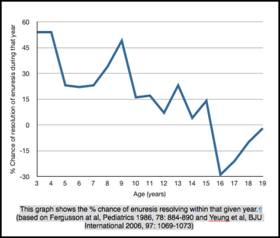
Figura 5
Un gran estudio epidemiológico basado en un estudio realizado por el grupo de CK Yeung en Hong Kong definió las tasas de prevalencia de la enuresis nocturna en niños y adolescentes (90). Una tasa de respuesta del 78,6% a los 21,000 cuestionarios reveló una prevalencia general de enuresis nocturna primaria del 3,1%, de los cuales el 20,7% también tenía incontinencia urinaria diurna. Demuestran muy elegantemente una marcada reducción en la incidencia global de la enuresis nocturna primaria con el aumento de la edad. Una tasa de prevalencia global del 16,1% a los 5 años de edad se había reducido al 10,1% a los 7 años, al 3,14% a los 9 años y al 2,2% a los 19 años. Hubo una marcada preponderancia masculina hasta los 7 años y, posteriormente, solo un ligero sesgo hacia que más niños sean afectados. Lo que no se desprende de este estudio es si esta resolución es "espontánea" o el resultado de una intervención médica / conductual. Los datos más interesantes que surgieron de ese estudio revelaron que la resolución espontánea probablemente solo se aplica a aquellos que tienen síntomas enuréticos leves, es decir, mojar <3 noches a la semana.
Tabla 1. También demostraron que los enuréticos adolescentes tienen una mayor prevalencia de enuresis nocturna no monosintomática que los menores de 10 años. (Adaptado de Yeung et al, BJU International 2006, 97: 1069–1073)
| 5 años de edad | 19 años | | |
|---|---|---|---|
| Prevalencia general | 16.1% | 2.2% | |
| % que mojaron <3 noches / semana | 55.7% | 10.3% | |
| % de personas que mojaron 3-6 noches / semana | 30% | 41.4% | |
| % de noches mojadas 7 / semana | 14,3% | 48.3% | |
Resultados a largo plazo / Gestión de adolescentes
Ha habido una serie de publicaciones que analizan el impacto psicológico y académico de la enuresis y la capacidad del tratamiento para mejorarlo. Informes anteriores han sugerido que los enuréticos no alcanzaron su potencial académico completo, pero eso se invierte después de la resolución de la enuresis. Sin embargo, un reciente estudio de gran población en el Reino Unido no encontró esto (92). Encontraron una asociación entre el orinarse en la cama y el aumento de la información sobre preocupaciones de los padres sobre tristeza / depresión, trastornos de la atención / actividad, trastornos de conducta, comportamiento de oposición y ansiedad general. A diferencia de los informes anteriores, no encontraron ninguna evidencia de un aumento en los problemas de comportamiento informados por los niños, como el acoso escolar / victimización, el rendimiento académico, la autoestima o las amistades.
"El manejo de la enuresis nocturna es un arte gratificante que requiere un médico entusiasta que esté dispuesto a usar una variedad de diferentes estratagemas con confianza según las necesidades particulares del niño y la familia" Roy Meadow, Arch Dis Child, 1974, 49: 257- 258
Referencias
- Bed-wetting. Kidney.org. http://www.kidney.org/patients/bw/index.cfm
- Bower, WF, Moore, KH, Shepherd, RB y Adams, RD La epidemiología de la enuresis infantil en Australia . BJU, 1996, 78: 602-606. http://www.ncbi.nlm.nih.gov/pubmed/8944518
- Butler, RJ, Golding, J., Northstone, K. y el equipo de estudio de APSPAC. Enuresis nocturna a los 7,5 años: prevalencia y análisis de los signos clí** nicos** . BJU International, 2005, 96: 404-410 http://www.ncbi.nlm.nih.gov/pubmed/16042739
- Yeung, CK, Sreedhar, B., Sihoe, JDY, Sit, FKY y Lau, J. Diferencias en las características de la enuresis nocturna entre niños y adolescentes: una evaluació** n cr **ítica de un gran estudio epidemioló** gico** . BJU International, 2006, 97: 1069-1073 http://www.ncbi.nlm.nih.gov/pubmed/16643494
- Chung, JM, Lee, SD, Kang, DD, Kim, KS, Kim, SY, Moon du, G., Park, KH, Pai, KS, Suh, HJ, Lee, JW, Cho, WY, Ha, TS y Han, SW Un estudio epidemiológico de la evacuación y los hábitos intestinales en niños coreanos: un estudio multicéntrico a nivel nacional . Urología, 2010, 76: 215-219. http://www.ncbi.nlm.nih.gov/pubmed/20163840
- Vande Walle, J. y Van Laecke, E. Pitfalls en estudios de niños con enuresis nocturna monosintomá** tica** . Pediatr Nephrol, 2008, 23: 173-178 http://www.ncbi.nlm.nih.gov/pubmed/18057964
- Norgaard, JP, van Gool, JD, Hjalmas, K., Djurhuus, JC y Hellstrom, A.-L. Estandarización y definiciones en la disfunción del tracto urinario inferior en niños . BJU, 1998, 81 (Suppl. 3): 1-16 http://www.ncbi.nlm.nih.gov/pubmed/9634012
- Neveus, T. y otros. La estandarización de la terminología de la función del tracto urinario inferior en niños y adolescentes: Informe del Comité de Normalizació** n de la International Children's Continence Society** . J Urol 2006, 176: 314-324 http://www.ncbi.nlm.nih.gov/pubmed/16753432
- Robson, WLM, Leung, AKC y Van Howe, R. Enuresis nocturna primaria y secundaria: similitudes en la presentación . Pediatría 2005, 115: 956-959. http://www.ncbi.nlm.nih.gov/pubmed/15805370
- von Gontard, A., Heron, J. y Joinson, C. Antecedentes familiares de enuresis nocturna e incontinencia urinaria: resultados de un gran estudio epidemioló** gico** . J Urol, 2011, 185 (6): 2303-2306 http://www.ncbi.nlm.nih.gov/pubmed/21511300
- Jarvelin, MR, Vikevainen-Tervonen, L., Moilanen, I. y Huttunen, N.-P. Enuresis en niños de siete años . Acta Paediatr Scand 1988, 77: 148 1. 153. http://www.ncbi.nlm.nih.gov/pubmed/3369293
- Wang, QW, Wen, JG, Zhu, QH, Zhang, GX, Yang, K., Wang, Y., Zhu, ZQ, Li, ZZ, Zhang, RL, Yang, YF y Wei, JX El efecto de la agregación familiar En los niños con enuresis nocturna primaria . Neurourol Urodyn 2009, 28 (5): 423-426 http://www.ncbi.nlm.nih.gov/pubmed/19012298
- Loeys, B., Hoebeke, P., Raes, A., Messiaen, L., De Paepe, A. y Vande Walle, J. ¿** Existe enuresis monosintom **á** tica? ** Una exploració** n gen **ética molecular de 32 familias con enuresis / incontinencia . BJU International 2002, 90: 76-83 http://www.ncbi.nlm.nih.gov/pubmed/12081775
- Eiberg, H., Berendt, I. y Mohr, J. Asignación de enuresis nocturna hereditaria dominante (ENUR1) al cromosoma 13q . Nature Genetics 1995, 10: 354-356 http://www.ncbi.nlm.nih.gov/pubmed/7670476
- Schaumburg, HL, Kapilin, U., Blasvaer, C., Eiberg, H., von Gontard, A., Djurhiuus, JC y Rittig, S. Fenotipos hereditarios en la enuresis nocturna . BJU International 2008, 102: 816-821 http://www.ncbi.nlm.nih.gov/pubmed/18564134
- von Gontard, A., Schaumburg, H., Hollmann, E., Eibery, H. y Rittig, S. La gen** ética de la enuresis: una revisión. ** J Urol 2001, 166: 2438-24434 http://www.ncbi.nlm.nih.gov/pubmed/11696807
- Butler, RJ y Holland, P. Los tres sistemas: una forma conceptual de entender la enuresis nocturna . Scand J Urol Nephrol 2000, 34 (4): 270-277 http://www.ncbi.nlm.nih.gov/pubmed/11095087
- Robertson, GL y Norgaard, NP Regulación renal del volumen de orina: posibles implicaciones para la nicturia . BJU International 2002, 90 (Suppl.3): 7-10 http://www.ncbi.nlm.nih.gov/pubmed/12445091
- Nielsen, S. Las acuaporinas renales: una visió** n general** . BJU International 2002, 90 (Suppl. 3): 1-6 http://www.ncbi.nlm.nih.gov/pubmed/12445090
- Nejsum, LN El sistema de plomería renal: canales de agua de acuaporina . CMLS, celular. Mol. Vida sci. 2005, 62: 1692-1706 http://www.ncbi.nlm.nih.gov/pubmed/15924268
- MacLean Poulton, E. Poliuria nocturna relativa como factor en la enuresis . The Lancet 1952, 8 de noviembre: 906-907 http://www.ncbi.nlm.nih.gov/pubmed/12991636
- Rittig, S., Knudsen, UB, Norgaard, JP, Pedersen, EB y Djurhuus, JC Ritmo diurno anormal de la vasopresina plasm** ática y gasto urinario en pacientes con enuresis** . Am J Physiol 1989, 256 (Electrolye Fluid Renal Fluid, 25): F664-F671 http://www.ncbi.nlm.nih.gov/pubmed/2705537
- Rittig, S., Matthiesen, TB, Pedersen, EB y Djurhuus, JC Variación circadiana de la angiotensina II y la aldosterona en la enuresis nocturna: Relación con la presión arterial y la producció** n de orina** . J Urol 2006, 176: 774-780 http://www.ncbi.nlm.nih.gov/pubmed/16813944
- Aceto, G., Penza, R., Delvecchio, M., Chiozza, ML, Cimador, M. y Caione, P. La tasa de excreción de fracciones de sodio en la enuresis nocturna se correlaciona con la poliuria nocturna y la osmolalidad . J Urol 2004, 171: 2567-2570 http://www.ncbi.nlm.nih.gov/pubmed/15118420
- Raes, A., Dossche, L., Hertegonne, N., Nuytemans, L., Hoebeke, P., Van Laecke, E., Donckerwolcke, R. y Vande Walle, J. Hypercalciuria est** á relacionada con la excreció **n osmolar en ni** ños con Enuresis nocturna** . J Urol 2010, 183: 297-301. http://www.ncbi.nlm.nih.gov/pubmed/19914655
- Valenti, G., Laera, A., Pace, G., Aceto, G., Lospalluti, ML, Penza, R., Selvaggi, FP, Chiozza, ML y Svelto, M. La acuaporina urinaria 2 y la calciuria se correlacionan con la gravedad De la enuresis en niños . J Am Soc Nephrol 2000, 11: 1873-1881 http://www.ncbi.nlm.nih.gov/pubmed/11004218
- Neveus, T., Hansell, P., y Stenberg, A. Vasopresina e hipercalciuria en la neuresis: una reaparici** ón** l. BJU International 2002, 90: 725-729 http://www.ncbi.nlm.nih.gov/pubmed/12410756
- Procino, G., Mastrofrancesco, L., Mira, A, Tamma, G., Carmosino, M., Emma, F., Svelto, M. y Valenti, G. Aquaporin 2 y receptor de detección de calcio apical: Nuevos jugadores en Trastornos poliuricos asociados a hipercalciuria . Seminarios en nefrología 2008, 28 (3): 297-305 http://www.ncbi.nlm.nih.gov/pubmed/18519090
- Rittig, S., Knudsen, UB, Norgaard, JP, Gregersen, H., Pedersen, EB y Djurhuus, JC Variació** n diurna del p **é** ptido natriur **ético auricular en plasma en pacientes normales y pacientes con enuresis nocturna . Scand J Clin Lab Invest 1991, 51: 209-217 http://www.ncbi.nlm.nih.gov/pubmed/1828306
- Kamperis, K., Hansen, MN, Hagstroem, S., Hvistend, G, Djurhuus, JC y Rittig, S. El ritmo circadiano de la producción de orina, y vasopresina urinaria y la excreció** n de prostaglandina E2 en ni **ños sanos . J Urol 2004, 171: 2571-2575 http://www.ncbi.nlm.nih.gov/pubmed/15118421
- Kamperis, K., Rittig, S., Jorgensen, KA y Djurhuus, JC Poliuria nocturna en la enuresis nocturna monosintomática refractaria al tratamiento con desmopresina . Am J Physiol Renal Physiol 2006, 291: F1232-F1240 http://www.ncbi.nlm.nih.gov/pubmed/16804103
- Salmon, MA Un relato histórico de la enuresis nocturna y su tratamiento . Proc Roy Soc Med 1975, 68: 443-445 http://www.ncbi.nlm.nih.gov/pubmed/801839
- Watanabe, H. y Azuma, Y. Una propuesta para un sistema de clasificación de enuresis basado en el monitoreo simultáneo durante la noche de la electroencefalografía y la cistometría . Sleep 1989, 12 (3): 257-264 http://www.ncbi.nlm.nih.gov/pubmed/2740698
- Watanabe, H., Kawauchi, A., Kitamori, T y Azuma, Y. Sistema de tratamiento para la enuresis nocturna según un sistema de clasificació** n original** . Eurolol 1994, 25: 43-50. http://www.ncbi.nlm.nih.gov/pubmed/8307075
- Yeung, CK, Sit, FKY, To, LKC, Chiu, HN, Sihoe, JDY y Wong, C. La reducción de la capacidad vesical funcional nocturna es un factor común en la patogenia de la enuresis nocturna refractaria . BJU International 2002, 90: 302-307 http://www.ncbi.nlm.nih.gov/pubmed/12133069
- Yeung, CK Enuresis nocturna (enuresis) . Curr Opin Urol 2003, 13: 337-343 http://www.ncbi.nlm.nih.gov/pubmed/12811299
- Hansen, MN, Rittig, S., Siggaard, C., Kamperis, K., Hvistendahl, G., Schaumburg, HL, Schmidt, F., Rawashdeh, Y. y Djurhuus, JC. Variabilidad intraindividual en la producción nocturna de orina y Capacidad funcional de la vejiga estimada por registros domiciliarios en pacientes con enuresis nocturna . J Urol 2001, 166: 2452-2455 http://www.ncbi.nlm.nih.gov/pubmed/11696810
- Oredsson, AF y Jorgensen, TM Cambios en la capacidad de la vejiga nocturna durante el tratamiento con la campana y la almohadilla para la enuresis nocturna monosintomá** tica** . J Urol 1998, 160: 166-169 http://www.ncbi.nlm.nih.gov/pubmed/9628642
- Norgaard, JP, Hansen, JH, Wildschiotz, G., Sorensen, S., Rittig, S. y Djurhuus, JC. Cistometrías del sueño en niños con enuresis nocturna . J Urol 1989, 141: 1156-1159 http://www.ncbi.nlm.nih.gov/pubmed/2709503
- Fowler, CJ, Griffiths, D. y de Groat, WC El control neuronal de la micción . Nat Rev Neurosci 2008, 9 (6): 453-466 http://www.ncbi.nlm.nih.gov/pubmed/18490916
- Holstege, G. E l sistema motor motor emocional y control de micciones . Neurourology and Urodynamics 2010, 29: 42-48 http://www.ncbi.nlm.nih.gov/pubmed/20025036
- Blok, BFM, Willemsen, ATM y Holstege, G. Un estudio PET sobre el control cerebral de la micción en humanos . Brain 1997, 120: 111-121 http://www.ncbi.nlm.nih.gov/pubmed/9055802
- Dobbing, J. and Sands, J. Crecimiento cuantitativo y desarrollo del cerebro humano . Arch Dis Child 1973, 48: 757-767 http://www.ncbi.nlm.nih.gov/pubmed/4796010
- Koff, SA **Cura de la enuresis nocturna: ¿por qué la desmopresina no es muy efectiva? ** Pediatr Nephrol 1996, 10: 667-670 http://www.ncbi.nlm.nih.gov/pubmed/8897581
- Jarvelin, MR Historia del desarrollo y hallazgos neurológicos en niños enuré** ticos** . Dev Med and Child Neur 1989, 31: 728-736 http://www.ncbi.nlm.nih.gov/pubmed/2599267
- von Gontard, A., Schmelzer, D., Seifen, S. y Pukrop, R. Compromiso del sistema nervioso central en la enuresis nocturna: evidencia de retraso neuromotor general y disfunción especí** fica del tronco cerebral** . J Urol 2001, 166: 2448-2451 http://www.ncbi.nlm.nih.gov/pubmed/11696809
- von Gontard, A., Freitag, CM, Seifen, S., Pukrop, R. y Rohling, D. Desarrollo neuromotor en la enuresis nocturna . Dev Med & Child Neur 2006, 48: 744-750 http://www.ncbi.nlm.nih.gov/pubmed/16904021
- Ornitz, EM, Russell, AT, Hanna, GL, Gabikian, P., Gehricke, JG., Song, D. y Guthrie, D. Inhibición de sobresalto del sobresalto y la neurobiología de la enuresis nocturna primaria . Biol Psychiatry 1999, 45: 1455-1466 http://www.ncbi.nlm.nih.gov/pubmed/10356628
-
Freitag, CM, Rohling, D., Seifen, S., Pukrop, R. y von Gontard, A. Neurofisiolog** ía de la enuresis nocturna: potenciales evocados e inhibición prepulso del reflejo de sobresalto** . Dev Med & Child Neurol 2006, 48: 278-284 http://www.ncbi.nlm.nih.gov/pubmed/16542515
- Wolfish, NM, Pivik, RT y Busby, KA Umbrales elevados de activación del sueño en niños enuréticos: implicaciones clí** nicas** . Acta Paediatr1997, 86: 381-384 http://www.ncbi.nlm.nih.gov/pubmed/9174224
- Cohen-Zrubavel, V., Kushnir, B., Kushnir, J. y Sadeh, A. El sueño y la somnolencia en niños con enuresis nocturna . Sleep 2011, 34 (2): 191-194 http://www.ncbi.nlm.nih.gov/pubmed/21286252
- Cinar, U., Vural, C., Cakir, B., Topuz, E., Karaman, MI y Turgut, S. ** Enuresis nocturna y obstrucció** n de la v **ía aérea superior** . Int J Pediatr Otorhinolaryngol 2001, 59: 115-118 http://www.ncbi.nlm.nih.gov/pubmed/11378186
- Robson, WLM y Leung, AKC Enuresis nocturna secundaria . Clin Pediatrics 2000, 39 (7): 379-385 http://www.ncbi.nlm.nih.gov/pubmed/10914301
- Neveus, T. Enuresis nocturna: antecedentes teóricos y directrices prácticas . Pediatr Nephrol 2011, 26: 1207-1214 http://www.ncbi.nlm.nih.gov/pubmed/21267599
- Thiedke, CC Enuresis nocturna . Am Fam Physcian 2003, 67: 1499-1506 http://www.ncbi.nlm.nih.gov/pubmed/12722850
- Moffatt, MEK Enuresis nocturna: implicaciones psicológicas del tratamiento y el no tratamiento . J Pediatr 1989, 114, (4, Parte 2): 697-704 http://www.ncbi.nlm.nih.gov/pubmed/2647952
- Hjalmas, K., Arnold, T., Bower, W., Caione, P., Chiozza, LM, von Gontard, A., Han, SW, Husman, DA, Kawauchi, A., LAckgren, G., Lottmann, H., Mark, S., Rittig, S., Robson, L., Vande Walle, J. y Yeung CK Enuresis nocturna: una estrategia de gestión internacional basada en la evidencia . J Urol 2004, 171: 2545-2561 http://www.ncbi.nlm.nih.gov/pubmed/15118418
- Cayan, S., Doruk, E., Bozlu, M., Duce, MN, Ulusoy, E. y Akbay, E. La evaluación del estreñimiento en la enuresis nocturna primaria monosintomá** tica** . Urología y nefrología internacionales 2001, 33: 513-516 http://www.ncbi.nlm.nih.gov/pubmed/12230285
- Marson, FGW Tratamiento de la pituitaria posterior de la enuresis nocturna . BMJ 1955, 14 de mayo: 1194-1195. http://www.ncbi.nlm.nih.gov/pubmed/14363834
- Richardson, DW, y Robinson, AG Desmopressin . Annals of Internal Medicine 1985, 103: 228-239 http://www.ncbi.nlm.nih.gov/pubmed/3893256
- Vande Walle, JGJ, Bogaert, GA, Mattsson, S., Schurmans, T., Hoebeke, P., Deboe, V. y Norgaard, JP Una nueva formulación oral de desmopresina de rá** pida fusi **ón: un estudio farmacodinámico en niños con enfermedad nocturna primaria La enuresis . BJU International 2006, 97: 603-609 http://www.ncbi.nlm.nih.gov/pubmed/16469035
- Glazener, CMA y Evans, JHC Desmopresina para la enuresis nocturna en niños . Base de Datos Cochrane de Revisiones Sistemáticas 2002, Número 3. Art. No. CD002112 http://www.ncbi.nlm.nih.gov/pubmed/12137645
- Alloussi, SH, Murtz, G., Lang, C., Madersbacher, H., Strugala, G., Seibold, J., Schwenter, C., Stenzl, A. y Alloussi, S. Reg** ímenes de tratamiento con desmopresina en monosintomático y no monosintomá **tico Enuresis: una revisi** ón desde la perspectiva clínica** . J Ped Urol 2011, 7: 10-20 http://www.ncbi.nlm.nih.gov/pubmed/20576470
- Marschall-Kehrel, D. y Harms, TW La abstinencia desmopresina estructurada mejora la respuesta y el resultado del tratamiento para los niños enuré** ticos monosintom **á** ticos** . J Urol 2009, 182: 2022-2027 http://www.ncbi.nlm.nih.gov/pubmed/19695616
- Vilhardt, H. y Lundin, S. Efecto biológico y concentraciones plasmáticas de dDAVP después de la administración nasal y peroral en humanos . Gen Pharmac 1986, 17 (4): 481-483 http://www.ncbi.nlm.nih.gov/pubmed/3758654
- Knudsen, UB, Rittig, S., Norgaard, JP, Lundemose, JB, Pedersen, EB y Djurhuus, JC Tratamiento a largo plazo de la enuresis nocturna con desmopresina. Un estudio de seguimiento . Urol Res 1991, 19: 237-240. http://www.ncbi.nlm.nih.gov/pubmed/1926658
- NICE guía clínica 111. Enuresis nocturna: el manejo de la enuresis en niños y jóvenes . www.nice.org.uk/guidance/CG111
- De Guchtenaere, A., Raes, A., Vande Walle, C., Hoebeke, P., Van Laecke, E., Donckerwolcke, R. y Vande Walle, J. Evidencia de respuesta anti-enurética parcial relacionada con efectos farmacodinámicos deficientes de desmopresina en spray nasal . J Urol 2009, 181: 302-309 http://www.ncbi.nlm.nih.gov/pubmed/19013601
- Althaus, J. Enuresis nocturna tratada por alternativas voltaicas . BMJ 1883, 20 de enero: 104 http://www.ncbi.nlm.nih.gov/pubmed/20750468
- Goel, KM, Thomson, RB, Gibb, EM y McAinsh, TF Evaluación de nueve tipos diferentes de alarmas de enuresis . Arch Dis Child 1984, 59: 748-753 http://www.ncbi.nlm.nih.gov/pubmed/6476872
- Glazener, CMA, Evans, JHC y Peto, RE Intervenciones de alarma para la enuresis nocturna en niños . Base de Datos Cochrane de Revisiones Sistemáticas 2005, Número 2 Art. No. CD002911 http://www.ncbi.nlm.nih.gov/pubmed/15846643
- Baeyens, D., Lierman, A., Roeyers, H., Hoebeke, P. y Vande Walle, J. Adherencia en niños con enuresis nocturna . J Ped Urol 2009, 5: 105-109 http://www.ncbi.nlm.nih.gov/pubmed/18996052
- Schulz-Jurgensen, S., Rieger, M., Schaefer, J., Neusuess, A. y Eggert, P. El efecto de la 1-desamino-8-d-arginina vasopresina en la inhibición prepulso del sobresalto apoya una etiología central de la monosintomática primaria La enuresis . J Pediatr 2007, 151: 571-574 http://www.ncbi.nlm.nih.gov/pubmed/18035131
- Glazener, CMA, Evans, JHC y Peto, RE Medicamentos para la enuresis nocturna en niños (que no sean desmopresina y tricíclicos ). Base de Datos Cochrane de Revisiones Sistemáticas 2003, Número 4 Art. No. CD002238 http://www.ncbi.nlm.nih.gov/pubmed/14583948
- Lovering, JS, Tallett, SE y McKendry, la eficacia de la oxibutinina en el tratamiento de la enuresis primaria . Pediatría 1988, 82 (1): 104-106 http://www.ncbi.nlm.nih.gov/pubmed/3288951
- Austin, PF, Ferguson, G., Yan, Y., Campigotto, MJ, Royer, ME y Coplen, DE Tratamiento combinado con desmopresina y un medicamento anticolinérgico para pacientes que no responden a la desmopresina para la enuresis nocturna monosintomá** tica: un estudio aleatorio, doble ciego, placebo -Control controlado** . Pediatría 2008, 122: 1027-1032 http://www.ncbi.nlm.nih.gov/pubmed/18977983
- MacLean, REG Clorhidrato de imipramina (tofranil) y enuresis . Am J Psychiatry 1960, 117: 551 http://www.ncbi.nlm.nih.gov/pubmed/13764959
- Glazener, CMA, Evans, JHC y Peto, RE Tricíclicos y fármacos relacionados para la enuresis nocturna en niños . Base de Datos Cochrane de Revisiones Sistemáticas 2003, Número 3 Art. No. CD002117 http://www.ncbi.nlm.nih.gov/pubmed/12917922
- Lundmark, E. y Neveus, T. Reboxetine en enuresis resistente a la terapia: una evaluación retrospectiva . Scand J Urol & Nephrol 2009, 43: 365-368 http://www.ncbi.nlm.nih.gov/pubmed/19921980
- Vogt, M., Lehnert, T., Till, H. y Rolle, U. Evaluación de diferentes modos de terapia combinada en niños con enuresis nocturna monosintomá** tica** . BJU International 2009, 105: 1456-1459 http://www.ncbi.nlm.nih.gov/pubmed/19764973
- al-Wailli, NS I supositorio de ndometacina para tratar la enuresis nocturna primaria: estudio doble ciego . J Urol 1989, 142 (5): 1290-1292 http://www.ncbi.nlm.nih.gov/pubmed/2681838
- Metin, A. y Aykol, N. Supositorio sódico de diclofenaco en el tratamiento de la enuresis nocturna primaria . Int Urol Nephrol 1992, 24 (2): 113-117 http://www.ncbi.nlm.nih.gov/pubmed/1624253
- Neveus, T. Johansson, E., Nydahl-Persson, K., Peterson, H. y Hansson, S. Tratamiento diurético para la enuresis nocturna . Scand J Urol Nephrol 2005, 39 (6): 474-478 http://www.ncbi.nlm.nih.gov/pubmed/16303723
- Iawwa, IA, Matani, YS, Saleh, AA y Al-Ghazo, MA Un ensayo controlado con placebo de los efectos de la hidroclorotiazida sobre la enuresis nocturna . Urol Int 2010, 84 (3): 319-324 http://www.ncbi.nlm.nih.gov/pubmed/20389163
- Bower, WF, Diao, M., Tang, JL y Yeung, CK Acupuntura para la enuresis nocturna en niños: una revisió** n sistem **ática y exploración de las razones . Neurourology and Urodynamics 2005, 24: 267-272. http://www.ncbi.nlm.nih.gov/pubmed/15791606
- Glazener, CMA, Evans, JHC y Cheuk, DKL. Intervenciones complementarias y misceláneas para la enuresis nocturna en niños . Base de Datos Cochrane de Revisiones Sistemáticas 2005, Número 2 Art. No. CD005230 http://www.ncbi.nlm.nih.gov/pubmed/15846744
- Alexopoulos, EI, Kostadima, E., Pagonari, I., Zintzaras, E., Gourgoulianis, K. y Kaditis, AG Asociación entre la enuresis nocturna primaria y el ronquido habitual en niños . Urología 2006, 68: 406-409 http://www.ncbi.nlm.nih.gov/pubmed/16904463
- Kalorin, CM, Mouzakes, J., Gavin, JP, Davis, TD, Feustel, P. y Kogan, BA La amigdalectomía no mejora la enuresis: resultados de un ensayo prospectivo controlado . J Urol 2010, 184: 2527-2532 http://www.ncbi.nlm.nih.gov/pubmed/21030049
- Fergusson, DM, Horwood, LJ y Shannon, FT Factores relacionados con la edad de obtención del control nocturno de la vejiga: un estudio longitudinal de 8 años . Pediatría 1986, 78 (5): 884-890 http://www.ncbi.nlm.nih.gov/pubmed/3763302
- Yeung, CK, Sreedhar, B., Sihoe, JDY Sit, FKY y Lau, J. Diferencias en las características de la enuresis nocturna entre niños y adolescentes: una evaluació** n cr **ítica de un gran estudio epidemioló** gico** . BJU International 2006, 97: 1069-1073 http://www.ncbi.nlm.nih.gov/pubmed/16643494
- Forsythe, WI y Redmond, A. Enuresis y tasa de curación espontánea. Estudio de 1129 enuréticos . Arch Dis Child 1974, 49: 259-263 http://www.ncbi.nlm.nih.gov/pubmed/4830115
- Joinson, C., Heron, J., Emond, A. y Butler, R. Problemas psicol** ógicos en niños con enuresis y humectación combinada (día y noche): un estudio realizado en el Reino Unido y basado en la población** . J Psicología pediátrica 2007, 32 (5): 605-616 http://www.ncbi.nlm.nih.gov/pubmed/17071625









